Содержание страницы
Более 85 % деталей тракторов, автомобилей и технологического оборудования различного рода производств выбраковывают при износе до 0,3 мм. Большинство таких деталей целесообразно восстанавливать нанесением гальванических покрытий, которые имеют ряд преимуществ по сравнению с другими способами восстановления:
- отсутствие термического воздействия на деталь, которое вызывает в ней нежелательные изменения структуры и механических свойств;
- получение покрытий с высокой точностью заданной толщины, что позволяет уменьшить до минимума припуск на последующую механическую обработку или совсем исключить ее;
- осаждение покрытий с заданными постоянными по толщине физикомеханическими свойствами;
- одновременное восстановление большого числа деталей (в ванну загружают десятки деталей), что снижает трудоемкость и себестоимость восстановления единицы изделия;
- возможность автоматизации процесса.
При восстановлении изношенных деталей из гальванических покрытий чаще всего применяют железнение, реже – хромирование, цинкование и никелирование.
1. Сущность электролитического осаждения металлов
Электролитическое осаждение металлов основано на явлении электролиза. Электролизом называются химические процессы, протекающие на электродах при прохождении через электролит электрического тока. Электролитами являются растворы солей, кислот и щелочей, проводящие электрический ток.
Схема электролиза показана на рис 1.
При растворении вещества в воде его молекулы диссоциируют (растворяются) на отрицательно и положительно заряженные ионы, находящиеся в хаотическом движении. Если в электролит погрузить электроды, подключенные к источнику постоянного тока, в электролите возникнет направленное движение ионов и ток. При этом положительно заряженные ионы (ионы металлов и водорода) будут перемещаться к отрицательному электроду – катоду, а отрицательно заряженные ионы (ионы металлоидов и кислотных остатков) – к положительному электроду – аноду.
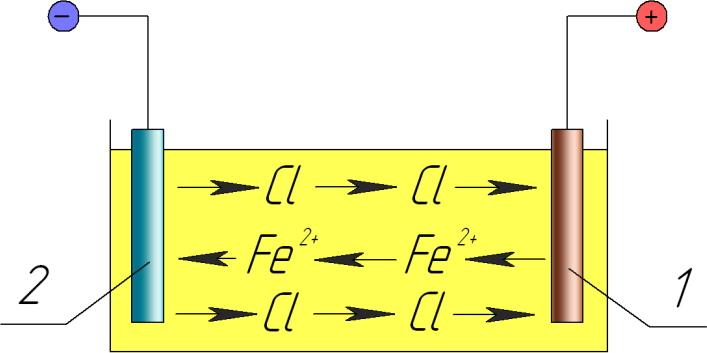
Рис 1. Схема процесса электролиза: 1 – анод; 2 – катод
По достижении поверхности электродов, ионы разряжаются и превращаются в нейтральные атомы или группы атомов. На катоде происходит осаждение металлов и выделение водорода. Анод как правило является растворимым, его ионы переходят в раствор, с выделением на поверхности анода кислорода.
При нанесении гальванических покрытий на детали в качестве электролитов используют растворы солей осаждаемых металлов. Также в электролит вводят определенные компоненты, улучшающие свойства покрытий, увеличивающие электропроводность электролита и т. д.
Детали, подлежащие покрытию, являются катодом, а анодом – пластины из осаждаемого металла. В некоторых процессах (например, при хромировании) используют аноды из металла или сплава, которые в электролите не растворяются (свинец), а также нерастворимые аноды из графита. На таких анодах при электролизе обычно происходит выделение кислорода.
В процессе электролиза ионы металла (катионы), находящиеся в электролите, разряжаются на катоде, переходят в атомарное состояние, и осаждаются на нем. Атомы образуют кристаллическую решетку, покрывая поверхность детали слоем металла. Анод растворяется (в случае электролиза с растворимым анодом), образуя новые ионы металла взамен выделившихся на катоде, тем самым поддерживая концентрацию электролита при электролизе.
Количественно процесс электролиза описывается двумя законами Фарадея, открытыми в 1833 г:
- Масса вещества, выделившегося на катоде или растворившегося на аноде, прямо пропорциональна силе тока и времени его прохождения, то есть прямо пропорциональна количеству прошедшего через электролит электричества.
- При прохождении одного и того же количества электричества через разные электролиты масса выделившихся или растворившихся веществ пропорциональна их химическим эквивалентам.
Оба закона Фарадея в общем виде выражают формулой
MT = C I t ,
где МT – масса выделившегося на катоде (растворившегося на аноде) вещества, г;
С – электрохимический эквивалент вещества, г/А·ч;
I – сила тока, проходящего через электролит, А;
t – продолжительность электролиза, ч.
Электрохимический эквивалент показывает, какое количество вещества выделится на катоде при пропускании через электролит 1 Ач электричества. При хромировании С = 0,323, а при железнении С = 1,042 г/(А· ч);
В процессе электролиза одновременно с осаждением металла на катоде выделяется водород, а также протекают и другие побочные процессы, на что потребляется часть электрического тока. Поэтому действительная масса осажденного металла всегда будет меньше теоретической, рассчитанной по закону Фарадея. Отношение практически полученного на катоде количества металла МП к теоретически возможному называется катодным выходом металла по току ηк , который выражают в процентах:
ηк = (МП / МТ) 100 % = (МП / С I t) 100 %
Выход металла по току является важнейшим показателем эффективности электролиза. Выход металла по току представляет собой коэффициент использования электрического тока (иногда его называют КПД ванны, что неверно, так как КПД характеризует использование энергии, а не тока). При железнении выход металла по току очень высок и составляет 85…95 %. Это означает, что 85…95 %, затраченного на электролиз, электричества полезно используется на осаждение металла.
Так же определяют и анодный выход по току – это отношение количества металла, практически растворенного на аноде, к теоретически возможному.
Режим электролиза определяется следующими, основными параметрами: состав и концентрация электролита, выраженная количеством граммов вещества, растворенного в 1 литре электролита, г/л;
кислотность электролита, выраженная в г/л или в единицах рН. Удобнее пользоваться водородным показателем, так как его легко определить, не производя химический анализ электролита, с помощью серийно выпускаемых приборов (рН-метров) или индикаторной бумаги;
температура электролита, °С;
катодная плотность тока, равная отношению силы тока, проходящего через электролит, к площади покрываемой поверхности.
Силу тока можно определить по формуле
I = Dк Fк,
где Dк – катодная плотность тока, при хромировании Dк = 50…75, при железнении Dк = 20…30 А/дм2;
Fк – площадь восстанавливаемой поверхности, дм2.
Продолжительность электроосаждения металлов в ванне рассчитывают по формуле
t = 1000 h γ / С Dк ηк,
где h – толщина покрытия, мм;
γ – плотность осажденного металла, при хромировании γ = 6,9 г/см3, при железнении γ = 7,8 г/см3;
Отношение площади анода к площади катода принимают равным 2 : 1. Изменяя условия электролиза можно управлять процессом электрокристаллизации металла и получать покрытия с заданными структурой и свойствами.
Если разделить толщину покрытия на продолжительность электролиза, то получим скорость осаждения металла или производительность процесса (мм/ч)
V = h / t = C Дк η / 1000 γ .
Так как электрохимический эквивалент вещества С и плотность осажденного металла зависят от природы осаждаемого металла и для каждого металла является постоянными, то скорость осаждения будет тем выше, чем выше плотность тока и выход по току. Поэтому при восстановлении деталей необходимо задавать как можно большую плотность тока, однако следует учитывать то, что при чрезмерном увеличении плотности тока требуемые свойства покрытия ухудшаются.
Электролитическое наращивание в зависимости от вида детали производят в установках 0013-006, 0013-022, 0013-024, 0013-31, 0013-040 «Ремдеталь». В качестве источников постоянного тока применяются либо низковольтные двигатель-генераторы типа АНД, либо выпрямители: селеновые типа ВСМН, ВСМР и др.; кремниевые типа ВАКГ и др.; германиевые типа ВАГГ, ВГВ и др.
Напряжение источников тока составляет 6…12 В.
2. Подготовка деталей к нанесению гальванических покрытий
Прочность сцепления гальванических покрытий зависит в основном от качества подготовки поверхности перед покрытием. Покрываемым поверхностям придают необходимую шероховатость, с них удаляют различные загрязнения, жировые и оксидные пленки. Если металл осаждается на активном чистом катоде, возникает межмолекулярное взаимодействие с основным металлом и покрытие не отслаивается от детали даже при ее разрушении. Нарушение технологии подготовки значительно снижает сцепляемость покрытия и приводит к его отслаиванию от детали.
Подготовка деталей к нанесению гальванических покрытий включает следующие операции:
- Очистка деталей от загрязнений на разборочно-моечном участке.
- Предварительная механическая обработка деталей для удаления следов износа, придания покрываемой поверхности правильной геометрической формы и шероховатости Ra 1,25…1 мкм.
- Промывка деталей синтетическим моющим средством (например 10 %-ный раствор МС-37 при температуре 70 °С) для удаления загрязнений.
- Изоляция поверхностей не подлежащих покрытию с помощью постоянных изоляторов (коробки, трубки, шайбы и т.д.) или различными изоляционными материалами: тонкой резиной, листовым целлулоидом, изоляционной лентой, пленочными полимерными материалами, церезином, пластизолем и др.
- Завешивание деталей на подвеску. Конструкция подвески должна создавать надежный электрический контакт с покрываемыми изделиями и штангой ванны.
- Обезжиривание химическим и электрохимическим методами.
К первому методу относится обезжиривание венской известью, представляющей собой смесь оксидов кальция и магния в соотношении 1 : 1. Ее разводят водой до кашицеобразного состояния, наносят на поверхность и протирают деталь волосяной щеткой. Это достаточно трудоемкая операция, однако обеспечивает высокое качество обезжиривания и оправдана при небольшой программе восстановления.
При электрохимическом обезжиривании детали, погруженные в щелочной раствор, включают в цепь электрического тока в качестве катода или анода. На поверхности электродов бурно выделяются пузырьки газа (водород на катоде, кислород на аноде), которые способствуют эмульгированию жиров и масел, механически разрывая и удаляя их пленки. Процесс обезжиривания ускоряется многократно. Скорость электрообезжиривания в основном зависит от плотности тока и незначительно от концентрации и температуры раствора. Плотность тока составляет 3…10 А/дм2, а температура раствора – 60…80 °С. Для обезжиривания черных металлов рекомендуется раствор, содержащий 30 г/л едкого натра, 30 г/л тринатрийфосфата и 40 г/л кальцинированной соды. В растворы можно вводить 3…5 г/л жидкого стекла или метасиликата натрия.
Обезжиривание ведут как на катоде, так и на аноде. Катодное обезжиривание более производительно, но приводит к наводороживанию деталей, что увеличивает их хрупкость и снижает усталостную прочность. Кроме того, ухудшается сцепляемость покрытия с поверхностью детали. Поэтому предпочтительна комбинированная обработка – обезжиривание на катоде в течение 4…5 мин, а затем переключают детали на анод и обезжиривают 1…2 мин.
- Промывка деталей горячей водой (70…80 °С).
- Промывка холодной водой.
- Анодное травление деталей. Операцию выполняют для удаления с поверхностей оксидных пленок и выявления кристаллической структуры металла. Состав электролита и режим обработки зависят от вида покрытия.
При железнении анодное травление проводят в 30-процентном растворе серной кислоты (365 г/л) и 10…20 г/л сернокислого железа (FeSO4 7Н2О) при температуре 18…25 °С. Детали завешивают на анодную штангу. Катодами служат свинцовые пластины, площадь которых в 4…5 раз превышает площадь покрываемых деталей. Стальные детали обрабатывают при плотности тока 30…50 А/дм2 в течение 2…3 мин, а чугунные – при 18…20 А/дм2 в течение 1,5…2 мин.
При хромировании анодное травление проводят в электролите, содержащем 100…150 г/л хромового ангидрида (CrO3) и 2…3 г/л серной кислоты (H2SO4), при анодной плотности тока Да = 25…40 А/дм2 в течение 30…90 с – для стальных деталей и при Да = 20…25 А/дм2 в течение 25…30 с – для чугунных деталей. Температура электролита 55…60 °С.
- Промывка холодной водой.
- Промывка горячей водой (60…70 °С).
3. Железнение
Железнение получило широкое применение при восстановлении деталей с износом от нескольких микрометров до 1,5 мм на сторону. Производительность процесса железнения примерно в 10 раз выше, чем при хромировании. Средняя скорость осаждения металла составляет 0,72…1 мкм/с, а выход металла по току равен 80…95 %.
По составу электролиты для железнения делят на три группы, которые различаются видом аниона соли железа: хлористые, сернокислые и смешанные (сульфатно-хлористые). Сернокислые электролиты по сравнению с хлористыми менее химически агрессивны и устойчивы к окислению. Однако они уступают хлористым электролитам по производительности, качеству получаемых покрытий и другим показателям.
По температуре электролиты делят на горячие и холодные. Горячие электролиты (процесс протекает при температуре электролита 60…95°C) производительнее холодных, но при работе с ними необходимы дополнительный расход энергии на поддержание высокой температуры электролита, частая его корректировка, дополнительная вентиляция и большая предосторожность со стороны рабочих.
Холодные электролиты устойчивее к окислению и покрытия получаются с лучшими механическими свойствами. В холодные электролиты вводится хлористый марганец, замедляющий образование дендритов и способствующий получению гладких покрытий большой толщины. Марганец на электроде не осаждается и сохраняется в электролите длительное время.
В табл 1 приведены наиболее распространенные составы электролитов и режимы железнения.
Таблица 1. Составы электролитов и режимы железнения
| Компонент и режим | Электролит | ||
| 1 | 2 | 3 | |
| Хлористое железо, г/л | 300…500 | 400…600 | 150…200 |
| Сернокислое железо, г/л | — | — | 200 |
| Аскорбиновая кислота, г/л | — | 0,5…2,0 | — |
| Кислотность (HCl), pH | 0,8…1,2 | 0,5…1,3 | 0,6…1,1 |
| Температура электролита, С | 70…80 | 20…50 | 30…50 |
| Плотность тока, А/дм2 | 20…50 | 10…30 | 20…25 |
| Выход по току, % | 85…95 | 85…92 | 85…92 |
Наибольшее распространение из вышеуказанных составов получил горячий хлористый электролит № 1.
Для обеспечения высокой прочности сцепления покрытий с деталями применяют разгонный режим: после промывки детали завешивают в ванну железнения и выдерживают без тока 10…60 с, затем включают ток плотностью 2…5 А/дм2 и проводят электролиз в течение 0,5…1 мин. Далее в течение 5…10 мин постепенно повышают катодную плотность тока до заданного значения. При железнении используют растворимые аноды из малоуглеродистой стали с содержанием углерода до 0,2 %. При электролизе аноды растворяются,
образуя на поверхности нерастворимый шлам, состоящий из углерода, серы, фосфора и других примесей. Попадая в ванну, они загрязняют ее и ухудшают качество покрытий. Во избежание этого аноды помещают в диафрагмы из пористой керамики или чехлы, сшитые из кислотостойкого материала (стеклоткань, шерсть и др.).
Соотношение площадей анодов и катодов Sа : Sk = 1 : 2, расстояние между ними 80…120 мм.
При определении необходимой толщины покрытия учитывают припуск на последующую механическую обработку, принимаемый равным 0,1…0,2 мм на диаметр для шлифования и 0,2…0,3 мм для токарной обработки.
Одним из основных недостатков процесса железнения является большое количество водорода в осадке, который в осадке находится в различных формах и отрицательно влияет на механические свойства восстановленных деталей. Поэтому рекомендуется детали после железнения подвергать низкотемпературному сульфидированию с последующей размерно-чистовой обработкой пластическим деформированием. В результате усталостная прочность деталей повышается на 40…45 %, а износостойкость возрастает в 1,5…2 раза.
Железнение проводят в стальных ваннах, внутренние стенки которых облицовывают кислотостойкими материалами (антегмитовая плитка АТМ-1, эмаль типа 105А, железокремниймолибденовый сплав МФ-15, кислотостойкая резина, фторопласт-3, керамика, фарфор). Стационарная ванна представляет собой емкость прямоугольной формы. В нее входят: нагревательное устройство (при необходимости), бортовые отсосы для удаления вредных испарений, катодные и анодные штанги, подсоединенные к источнику тока, для завешивания деталей и анодов.
При восстановлении крупногабаритных деталей сложной конфигурации (блоки цилиндров, картеры коробок передач и задних мостов, коленчатые валы и другие) возникают трудности, связанные с изоляцией мест, не подлежащих покрытию (площадь их поверхности в десятки раз превышает покрываемую площадь), сложной конфигурацией подвесных устройств, необходимостью иметь ванны больших размеров, быстрым загрязнением электролитов и т.д.
Для железнения таких деталей применяют вневанный способ. Сущность способа заключается в том, что в зоне нанесения покрытия создается местная ванночка, в которую подают электролит, а деталь и анод подключают к источнику тока. При этом непокрываемые поверхности не изолируют, уменьшается обеднение прикатодного слоя электролита и возможно увеличение плотности тока в несколько раз и, следовательно, повышение производительности процесса.
Способы вневанного осаждения металлов.
К безванным способам относят: проточный, струйный, электроконтактный и другие способы.
Проточный способ. При этом способе электролит прокачивают насосом с определенной скоростью через пространство между покрываемой поверхностью и анодом (например, через отверстие в корпусе коробки передач). Наибольшая скорость осаждения металлов наблюдается при скорости протекания электролита более 1 м/с, создающей турбулентный режим течения. Плотность тока может быть увеличена в 5…10 раз (при железнении – до 200…300 А/дм2 и более).
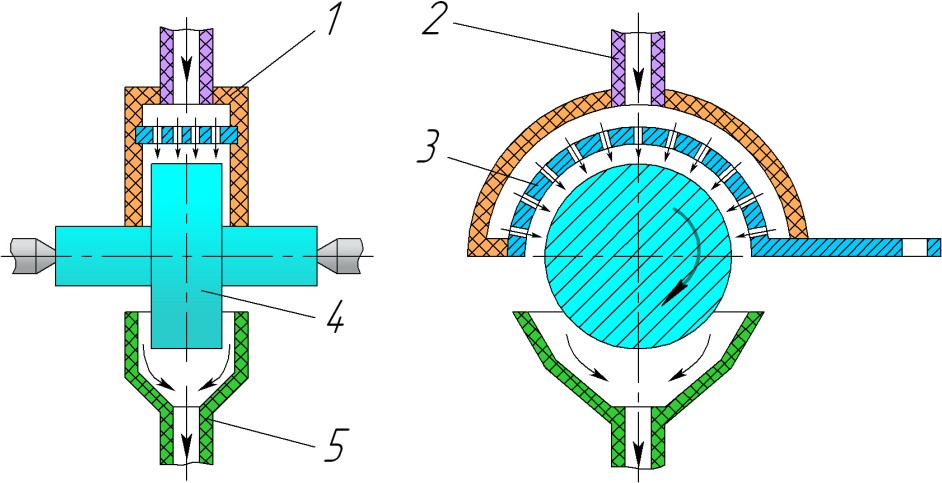
Струйное железнение. Электролит с помощью насоса подают струями в подводящий штуцер 2 (рис 2, а) межэлектродное пространство через отверстия насадка. Насадок одновременно служит анодом 3 и местной ванночкой. Для получения равномерного покрытия деталь 4 вращается с частотой до 20 мин-1. При использовании концентрированного холодного хлористого электролита и плотности тока DK = 40…55 А/дм2, производительность составляет 0,4 мм/ч.
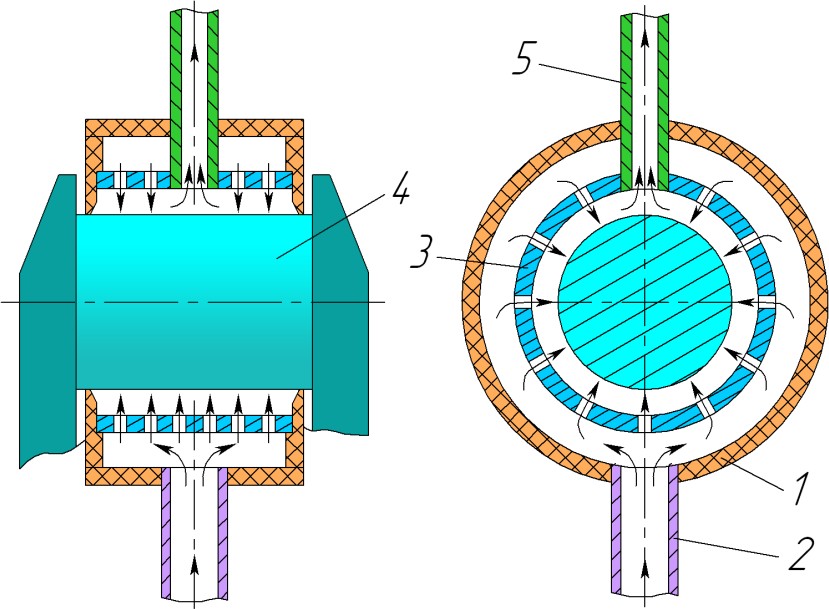
Для упрощения технологического процесса применительно к ремонту шеек коленчатых валов разработана электролитическая ячейка 1 (рис 2, б), которая дает возможность вести железнение и хромирование шеек без вращения детали. В эту ячейку электролит поступает под давлением через патрубок 2 и благодаря наклонному расположению отверстий в цилиндрическом аноде 3 (под углом 30…40° к радиальному направлению) приобретает вращательное движение вокруг детали 4. Скорость протекания электролита в аноднокатодном пространстве принимают 100…150 см/с при удельном его расходе 40…45 л/мин на 1 дм2 покрываемой поверхности.
а)
б)
Рис 2. Схема электролитических ячеек для струйного осаждения металлов c вращением (а) и без вращения детали (б): 1– корпус; 2 – подводящий штуцер; 3 – анод; 4 – деталь; 5 – сливной штуцер
При проточном и струйном способах меньше обеднение прикатодного слоя электролита, возможно увеличение плотности тока в несколько раз, что позволяет повысить производительность процесса в 2…3 раза. Способы обеспечивают более высокое качество покрытий и лучшую равномерность. Первым способом восстанавливают посадочные поверхности корпусных деталей (блоков цилиндров, корпусов коробок передач и др.), а вторым – крупные валы, например коленчатые.
Местное осаждение. В данном способе осаждение производят при неподвижном электролите. С помощью приспособлений изношенное отверстие детали превращается в закрытую местную гальваническую ванночку (рис 3). В центр ванночки устанавливают анод 3. Отверстие герметизируют снизу, заливают в него электролит, анод и деталь при этом неподвижны. При их подключении к источнику постоянного тока на поверхности отверстия осаждается железо. Температура электролита составляет 75…80 °С, катодная плотность тока – 25…30 А/дм2. Осаждаются качественные гладкие покрытия со скоростью 0,3 мм/ч, толщиной до 0,7 мм и твердостью 4000…4500 МПа. Этот способ часто применяют для восстановления посадок под подшипники в корпусных деталях. Электронатирание. При этом способе осаждения металла деталь 2 устанавливают в центрах (патроне) товарного станка и присоединяют к катоду источника постоянного тока (рис 4). Анодами служат металлические ролики 1, которые вращаясь совместно с деталью приводят в движение ленточный тампон 4, изготовленный из адсорбирующего материала. Необходимое усилие прижатия ленточного тампона к детали обеспечивает натяжной ролик 5. В системе катод (деталь) – тампон (своего рода гальваническая ванна) – анод (ролики) протекает электрохимическая реакция и на поверхности катода (детали) осаждается тот или другой металл. Тампон в зависимости от требуемого покрытия постоянно пропитывается электролитом из крана 4. Излишки электролита собираются в поддоне для повторного использования, откуда, очищаясь в фильтре, поступают в бак. Насос закачивает электролит в распределительный стакан при его опорожнении.
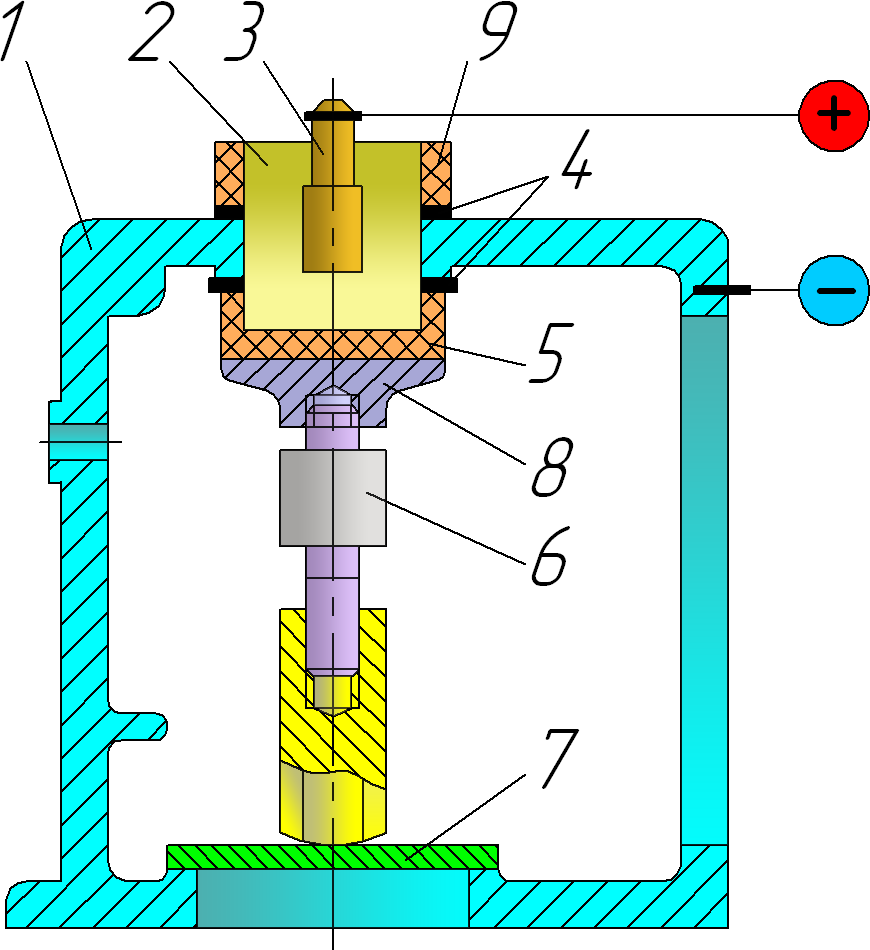
Рис 3. Схема местного железнения: 1 – деталь (корпус коробки передач); 2 – электролит; 3 – анод; 4 – резиновые прокладки; 5 – стакан; 6 – раздвижная распорка; 7 – опорная плита; 8 – подставка; 9 – кольцо
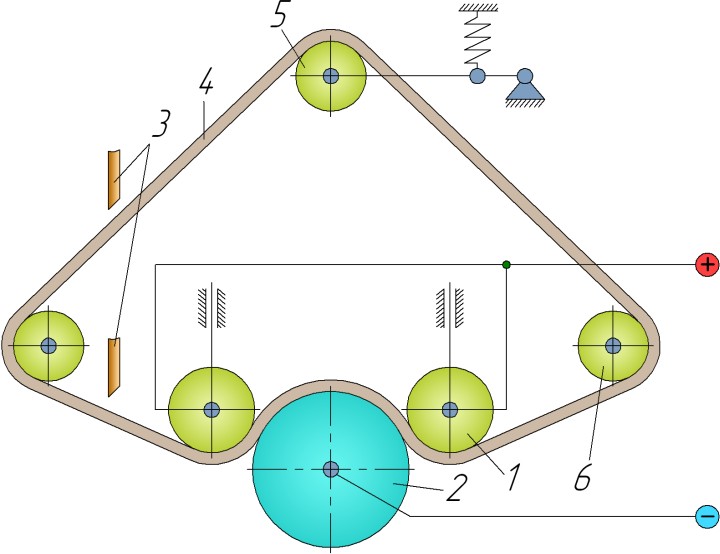
Рис 4. Принципиальная схема электроконтактного железнения: 1 – анод; 2 – катод (деталь); 3 – трубки подачи электролита; 4 – ленточный тампон; 5, 6 – натяжной и направляющий ролики
Постоянное поступление в зону электролиза свежего электролита и перемещение анода по покрываемой поверхности препятствуют росту зародившихся кристаллов металла, снижают внутренние напряжения в покрытии и уменьшают дендритообразование. Все это позволяет получать мелкозернистые покрытия высокого качества.
Состав электролита включает сульфат (250…300 г/л) и хлорид (130…150 г/л) железа. Режим процесса: рН 0,9…1,2; средняя катодная плотность тока 20…60 А/дм2; скорость вращения катода 20…40 м/мин; расход электролита 0,3…0,6 л/мин; угол обхвата детали тампоном 90…120°. Скорость осаждения составляет 3,3…12,3 мкм/мин. Микротвердость покрытия составляет 5500…7000 МПа. Так как покрытие получают гладким и равномерным, при толщине покрытия до 0,1 мм не требуется последующая механическая обработка.
Этот способ железнения рекомендуется применять для восстановления посадочных поверхностей крупных валов, осей и корпусных деталей.
4. Хромирование
Хромирование широко применяют для восстановления деталей, а также для получения декоративных и антикоррозионных покрытий.
Преимущества хромирования по сравнению с другими способам: покрытия электролитического хрома имеют: серебристо – белый цвет и высокую микротвердость 400…1200 МН/м2 (в 1,5…2 раза выше, чем при закалке ТВЧ), близкую к микротвердости корунда; обладают высокой износостойкостью (в 2…3 раза выше по сравнению с закаленной сталью); устойчивость к химическим и температурным воздействиям, причем высокая коррозионная стойкость сочетается с красивым внешним видом; имеют низкий коэффициент трения (на 50 % ниже, чем у стали и чугуна); высокую прочность сцепления покрытия с поверхностью детали.
Недостатками хромирования являются: низкий выход металла по току (8…42 %); небольшая скорость отложения осадков (0,03 мм/ч); большая трудоемкость и себестоимость наращивания; высокая агрессивность электролита; большое количество токсичных выделений, образующихся при электролизе; толщина отложения покрытия практически не превышает 0,3 мм.
В зависимости от назначения хромового покрытия применяются различные концентрации электролитов и режимы электролиза. Наибольшее применение получил так называемый универсальный электролит:
- хромовый ангидрид (CrО3) – 200…250 г/л;
- серная кислота (H2SO4) – 2…2,5 г/л.
Изменяя режим электролиза, из этого электролита можно получать все виды хромовых покрытий: блестящие, молочные и серые.
Блестящий хром характеризуется высокой микротвердостью (600…900 МН/м2), мелкой сеткой трещин, видимой под микроскопом. Осадки хрупкие, но с высокой износостойкостью. Молочный хром характеризуется пониженной микротвердостью (400…600 МН/м2), пластичностью и высокой коррозионной стойкостью. Серый хром отличается весьма высокой микротвердостью (900…1200 МН/м2) и повышенной хрупкостью, что снижает его износостойкость.
При восстановлении изношенных деталей, работающих в соединениях при давлениях до 0,5 МПа, применяются блестящие износостойкие покрытия, получаемые при плотности тока 30…100 А/дм2 и температуре электролита 50…70 °С (наиболее часто применяют Т = 55 ± 1 °С и Дk = 40…60 А/дм2).
В качестве защитно-декоративных применяются блестящие покрытия, получаемые при Дk = 15…25 А/дм2 и Т = 50 °С. Молочные покрытия, полученные при Дk = 25…35 А/дм2 и Т = 70 °С, обладают наибольшей коррозионной стойкостью, вязкостью, пониженным коэффициентом трения и применяются в качестве защитных покрытий, а также для восстановления деталей, работающих в тяжелых условиях: при высоких динамических нагрузках, при абразивном изнашивании в коррозионной среде и др. Колебание температуры электролита в процессе хромирования допускается в пределах ±1…2 °С.
При хромировании необходимо выдерживать соотношение анодной и катодной поверхностей Sa : Sk = 1,5…2, а расстояние между анодом и деталью – 30…35 мм.
В отличие от других гальванических процессов, при хромировании применяются нерастворимые аноды, изготавливаемые из свинца или сплава свинца с 6 % сурьмы. Поэтому электролит постоянно обедняется и его необходимо периодически корректировать, добавляя в него хромовый ангидрид.
В хромовом покрытии возникают растягивающие напряжения, значения которых растут с увеличением толщины покрытия. При определенной толщине растягивающие напряжения достигают таких значений, которые приводят к отслоению покрытия. Поэтому хромирование целесообразно применять для восстановления деталей при толщине покрытия до 0,3 мм. При определении необходимой толщины покрытия учитывают припуск на последующую механическую обработку, принимаемый равным 0,05…0,15 мм на диаметр.
В табл 2 приведены составы электролитов и режимы хромирования.
Таблица 2. Составы электролитов и режимы хромирования
| Компонента и режим | Номер | электролита | |||
| 1 | 2 | 3 | 4 | ||
| Хромовый ангидрид, г/л | 120…150 | 200…250 | 300…350 | 380…420 | |
| Серная кислота, г/л | 1,2…1,5 | 2,0…2,5 | 3,0…3,5 | – | |
| Сернокислый стронций, г/л | – | – | – | – | |
| Кремнефтористый калий, г/л | – | – | – | – | |
| Углекислый кальций, г/л | – | – | – | 40…60 | |
| Сернокислый кобальт, г/л | – | – | – | 18…20 | |
| Температура электролита, оС | 50…65 | 45…60 | 40…50 | 18…25 | |
| Плотность тока, А/дм2 | 30…100 | 20…60 | 15…30 | 100…300 | |
| Выход по току, % | 15…18 | 12…14 | 12…18 | 35…40 | |
Электролит № 1 имеет лучшую рассеивающую способность и более высокий выход по току, чем электролиты № 2 и № 3. Покрытия из этого электролита отличаются наибольшей твердостью и износостойкостью. Электролит применяют при восстановлении деталей, когда требуется высокая износостойкость.
Электролит № 2 называют универсальным, так как из него получают износостойкие покрытия и покрытия с защитно-декоративными свойствами.
Электролит № 3 используют при защитно-декоративном хромировании деталей сложной конфигурации.
Саморегулирующийся холодный электролит № 4 имеет наиболее высокие выход по току и скорость осаждения хрома, которая до 10 раз превышает скорость осаждения из обычных электролитов. Покрытия имеют хорошее качество.
Специальные процессы хромирования.
Пористое хромирование. Способ применяют для повышения износостойкости деталей, работающих при больших давлениях и температурах, а также в условиях недостаточной смазки. Пористый хром представляет собой покрытие с большим количеством пор или сеткой трещин, достаточно широких для проникновения в них масла. Данный вид покрытия можно получить механическим, химическим и электрохимическим способами. Наиболее широко применяют электрохимический способ, который заключается в том, что хром осаждают при режиме блестящего хромирования, в результате чего в покрытии появляются сетки микротрещин. Для их расширения и углубления покрытие подвергают анодной обработке в электролите того же состава.
Изменяя режимы хромирования и анодного травления можно получить пористость двух типов: канальчатую и точечную.
Для получения пористых покрытий деталь хромируют в универсальном электролите при плотности тока 40…50 А/дм2, а затем переключают полярность ванны и проводят анодное травление при той же плотности тока.
Канальчатую пористость получают при температуре электролита 58…62 °С и продолжительности травления 6…9 мин, а точечную – при 50…52 °С и 10…12 мин. Пористые покрытия применяют при размерном хромировании, например поршневых колец. Толщина пористых покрытий составляет 0,1…0,15 мм. Износостойкость поршневых колец с пористыми покрытиями увеличивается в 2…3 раза, а износостойкость гильзы цилиндров двигателя – в 1,5 раза.
Детали после покрытия пористым хромом подвергают термообработке в масле при температуре 150…200 °С в течение 1,5…2 ч для устранения водородной хрупкости и насыщения пор маслом.
Струйное хромирование. Процесс проводят в саморегулирующемся электролите при температуре 50…60 °С и плотности тока, достигающей 200 А/дм2. Скорость протекания электролита 40…60 см/с, катодно-анодное расстояние – 15 мм. В результате получают блестящие покрытия. Выход по току достигает 22 %, что вместе с высокой плотностью тока ускоряет процесс осаждения хрома. При температуре 50 °С и катодной плотности 100 А/дм2 скорость осаждения составляет 0,1 мм/ч. При струйном хромировании в тетрахроматном электролите и катодной плотности 150…160 А/дм2 высококачественные покрытия осаждаются со скоростью 0,25 мм/ч. В случае использования универсального электролита процесс осуществляют при температуре 50 °С, плотности тока 70…90 А/дм2, скорости протекания электролита 100…120 см/с, катодно-анодном расстоянии 15 мм. Скорость осаждения хрома при этом составляет 0,08…0,10 мм/ч.
Проточное хромирование. Данным способом получают блестящие покрытия повышенной твердости и износостойкости, а также повышенной равномерности покрытия. Процесс осуществляют в универсальном электролите с повышенным содержанием серной кислоты (3…7 г/л) при температуре 55…65 оС, плотности тока 100…150 А/дм2, скорости протекания электролита 100…120 см/с и межэлектродном расстоянии 15…30 мм. Выход по току составляет 20…21 %. Способ рекомендуется для хромирования цилиндров и коленчатых валов двигателей.
5. Обработка деталей после наращивания
После нанесения гальванического покрытия выполняют следующие операции:
- Промывка горячей водой (60…70 °С).
- Нейтрализация деталей для предотвращения коррозии в 10 %-ном растворе тринатрийфосфата при температуре 70…80 °С в течение 3…5 мин.
- Промывка горячей водой (70…80 °С).
- Демонтаж деталей с подвесок и снятие изоляции.
- Контроль качества покрытий.
- Механическая обработка до необходимого размера и шероховатости поверхности.

