Содержание страницы
1. Теория сплавов
Чистые металлы относительно редко применяют в машиностроении, так как не обеспечивают необходимого комплекса механических и технологических свойств изготовляемых из них деталей. Широко используют сплавы, состоящие из двух и более элементов (из двух металлов, например меди и цинка, или из металла и неметалла, например железа и углерода).
Элементы, входящие в сплав, называют компонентами.
Сплавы получают сплавлением компонентов, спеканием, электролизом и возгонкой. Компоненты, входящие в сплав, в жидком состоянии почти всегда растворяются друг в друге, образуя жидкий раствор. Атомы такого раствора равномерно перемешаны друг с другом. Свойства сплавов зависят главным образом от взаимодействия компонентов при затвердевании. При затвердевании сплавов образуется твердый раствор, химическое соединение или механическая смесь.
Твердый раствор. При переходе в твердое состояние в сплавах сохраняется однородность распределения атомов различных компонентов, а следовательно и свойство растворимости. При кристаллизации сплава атомы компонентов входят в единую ячейку кристаллической решетки, поэтому получаются однородные и одинаковые по составу зерна. Твердый раствор, как и чистый металл, имеет однообразную кристаллическую решетку. В кристаллической решетке чистого металла все узлы заняты атомами одного компонента, а в решетке твердого раствора — атомами компонентов, составляющих сплав. В твердых растворах растворимость компонентов не ограничена при любом их количественном соотношении (медь с никелем).
Свойства сплавов, образующих твердые растворы, изменяются плавно и отличаются от свойств компонентов, из которых они стоят. Они отличаются ценными свойствами. Они тверже и прочнее, чем входящие в них компоненты, обладают хорошей пластичностью, высоким электросопротивлением, не изменяющимся при изменении температуры, повышенным сопротивлением к коррозии. Благодаря высокой пластичности такие сплавы хорошо обрабатываются давлением.
Химическое соединение. Компоненты некоторых сплавов при кристаллизации могут входить в химическую связь, образуя химическое соединение. Например, железо с углеродом образуют химическое соединение Fe3C — карбид железа (цементит); медь с магнием — Cu2Mg; магний со свинцом — Mg2Pb и др.
Химическое соединение, как и твердый раствор, обладает однородной структурой. Кристаллическая решетка его включает атомы обоих компонентов. Однако в кристаллической решетке химического соединения, в отличие от твердого раствора, атомы каждого компонента находятся в строго определенном количестве и расположены всегда одинаково. Например, химическое соединение железа с углеродом Fe3C всегда состоит из трех атомов железа и одного атома углерода, соединение Mg2Pb всегда имеет два атома магния и один атом свинца. Таким образом, химическое соединение имеет постоянный состав и выражается химической формулой, а состав твердых растворов изменяется в широких пределах, твердый раствор не может быть выражен химической формулой. Кристаллическая решетка химического соединения отличается от решеток входящих в него компонентов, поэтому при образовании сплава оно рассматривается как самостоятельный компонент. Например, сталь — сплав, одним компонентом которого является железо, а другим — химическое соединение Fe3C (цементит).
Химические соединения обладают очень высокой твердостью и хорошим электросопротивлением. Иногда их твердость в 10 раз превышает твердость чистых компонентов. Так, например, железо с углеродом образует химическое соединение Fe3C, твердость которого в 10 раз выше твердости железа. Химические соединения вольфрама и титана с углеродом (карбиды), отличающиеся очень высокой твердостью, используются для изготовления режущих инструментов. В отличие от твердых растворов химические соединения характеризуются высокой хрупкостью, для обработки давлением они непригодны.
Механическая смесь. Отдельные компоненты в твердом состоянии не растворяются друг в друге (с образованием твердого раствора) и не входят между собой в химическую реакцию (с образованием химического соединения). При кристаллизации у каждого из таких компонентов создается своя, свойственная только ему одному кристаллическая решетка. Перемешиваясь друг с другом при постоянной температуре и определенном процентном соотношении, они образуют механическую смесь, в которой при рассмотрении под микроскопом видны отдельные компоненты. Так, механическая смесь РЬ — Sb образуется при температуре 246°С и соотношении компонентов: РЬ -87%, Sb—13%.
Механические смеси имеют хорошие литейные свойства. Особенно это относится к эвтектическим сплавам, которые обладают большей жидкотекучестью и меньшей температурой плавления, чем составляющие их компоненты.
Знание строения сплавов облегчает их выбор при изготовлении деталей машин и разработке технологических процессов. При изучении процессов, происходящих в металлах и сплавах в случае изменения их температуры и состава, пользуются такими понятиями, как компонент, система, фаза.
Системой в термодинамике называют совокупность веществ или тел, между которыми может беспрепятственно проходить обмен энергией и массой. В качестве системы может выступать химический элемент (сера, алюминий, водород), химическое соединение (Fe3C, вода, поваренная соль), сплав двух и более металлов (медь- никель, олово — свинец — сурьма), водный раствор (сахар в воде), смесь газов (воздух, состоящий из азота, кислорода, углекислого газа и пяти инертны газов).
Фазой называется часть системы, имеющая однородное строение и отделенная от других частей поверхностью раздела. В состав фазы может входить любое число компонентов, из которых состоит система. Система может содержать одну фазу и более. Однокомпонентные системы «сера», «алюминий», «поваренная соль» при комнатной температуре имеют одну твердую фазу, система «вода» в этих же условиях содержит одну жидкую фазу, а система «водород» — одну газообразную фазу. При температурах ниже нуля система «вода» также однофазна, имеет одну твердую фазу — лед. При нуле градусов эта система двухфазна, так как при этой температуре сосуществуют жидкая (вода) и твердая (лед) фазы.
Двухкомпонентная система «раствор сахара в воде» — однофазная, т. е. имеет одну жидкую фазу, если раствор ненасыщенный. Эта же система будет двухфазной при насыщенном растворе, содержащем нерастворившиеся кристаллы сахара, которые являются второй (твердой) фазой. Жидкая фаза в данном случае будет содержать два компонента (воду и сахар), а твердая только один (сахар).
2. Железоуглеродистые сплавы
2.1 Структурные составляющие железоуглеродистых сплавов
Чугун и сталь — основные машиностроительные материалы. Они составляют 95% всех используемых в технике сплавов.
Чугун — сплав на железной основе. Принципиальное отличие чугуна от стали заключается в более высоком содержании в нем углерода (более 2,14%). Наибольшее распространение получили чугуны, содержащие 3- 3,5% углерода. В состав чугунов входят те же примеси, что и в сталь, т. е. кремний, марганец, сера и фосфор, но в несколько больших количествах. Углерод в чугуне может находиться в химическом соединении с железом либо в свободном состоянии в виде графита. Чугуны, у которых весь углерод находится в химическом соединении с железом, называют белыми (по виду излома), а чугуны, весь углерод которых или большая его часть представляют собой графит, получили название серых.
Сталь — сплавы железа с углеродом и другими элементами, содержащие до 2,14% углерода. Углерод — важнейшая примесь стали. От его содержания зависят прочность, твердость и пластичность стали. Кроме железа и углерода в состав стали входят кремний, марганец, сера и фосфор. Эти примеси обычно попадают в сталь в процессе выплавки и являются ее неизбежными спутниками. Если марганец и кремний необходимы по условиям технологии выплавки, то сера и фосфор относятся к вредным примесям, не поддающимся полному удалению. В малом количестве в стали постоянно присутствуют скрытые примеси: кислород, водород, азот. Чем меньше вредных примесей, тем выше качество стали. Различают стали обыкновенного качества, качественные, высококачественные и особо высококачественные.
В железоуглеродистые сплавы входят различные структурные составляющие, свойства которых обусловливают свойства стали и чугуна.
Феррит — твердый раствор небольшого количества углерода (до 0,04%) и других примесей в железе — мягкая, пластичная и недостаточно прочная структурная составляющая. Его относительное удлинение 5 =30%, твердость — 50÷80 НВ, предел прочности σв = 300 МПа (30 кгс/мм2). Практически это чистое железо. Механические свойства феррита в большой степени зависят от величины зерен. Феррит обладает магнитными свойствами (до температуры 768 °С).
Цементит (Fe3C) — химическое соединение железа с углеродом — карбид железа. Он содержит 93,33% железа и 6,67% углерода, отличается большой твердостью (800 НВ, т. е. в 10 раз тверже феррита) и значительной хрупкостью. Цементит слабо магнитен, а при температурах выше 215 °С — немагнитен. Углерод может проникать в железо двумя способами. Атомы углерода могут занимать в пространственной решетке свободные места между атомами железа. Однако при комнатной температуре в пространственной решетке железа может поместиться всего 0,0001 % углерода. Остальные атомы углерода проникают в железо другим путем — вступают с ним в химическую связь. При этом образуется карбид железа Fe3C (цементит), состоящий из трех атомов железа и одного атома углерода.
Феррит и цементит являются основными структурными составляющими железоуглеродистых сплавов. Они могут располагаться, например, в структуре стали каждый в отдельности или в виде равномерной механической смеси, которая называется перлитом. Такое название эта смесь получила потому, что шлиф ее при травлении имеет перламутровый отлив. Так как перлит образуется в результате процессов вторичной кристаллизации, его называют эвтектоидом (в отличие от эвтектики). Образование перлита происходит при температуре 727 °С. В нем содержится 0,8% углерода.
Перлит имеет две разновидности. Если цементит в нем расположен в виде пластинок, его называют пластинчатым, если же цементит расположен в виде зерен, перлит называют зернистым. Под микроскопом пластинки цементита кажутся блестящими, потому что обладают большой твердостью, хорошо полируются и при травлении кислотами разъедаются меньше, чем пластинки мягкого феррита. После травления можно наблюдать темные участки перлита в сочетании с ферритом или цементитом. Поскольку перлит состоит из феррита и цементита, его свойства определяются количеством этих составляющих. Феррита содержится в перлите в шесть раз больше, чем цементита. Механические свойства перлита зависят также от формы цементита. У пластинчатого перлита твердость составляет 180÷200 НВ, предел прочности σв — 800 МПа (80 кгс/мм2), относительное удлинение δ = 10÷12%. У зернистого перлита прочность и твердость несколько ниже, а пластические свойства выше. Так как перлит содержит железо, он обладает магнитными свойствами.
Если железоуглеродистые сплавы нагреть до определенных температур, произойдет аллотропическое превращение железа и образуется структурная составляющая, которая называется аустенитом.
Аустенит представляет собой твердый раствор углерода (до 2,14%) и других примесей в железе. Способность углерода растворяться в железе неодинакова при различных температурах. При температуре 1147 °С и выше в кристаллической решетке у железа может раствориться максимальное количество углерода (2,14%). При температурах ниже 1147 °С растворимость углерода в железе постепенно уменьшается, а избыточный углерод выделяется в виде цементита. При 727 °С железо может растворять не более 0,8% углерода. При этой температуре происходит распад аустенита с образованием перлита. Лишь в некоторых сталях, содержащих большое количество никеля или марганца, структура аустенита .может сохраниться и при температурах ниже 727 °С (вплоть до комнатной). Аустенит — мягкая структурная составляющая (хотя и тверже феррита). Его твердость — 180 НВ, относительное удлинение δ = 40÷50%. Он отличается большой пластичностью, магнитными свойствами не обладает.
В белых чугунах всегда имеется еще одна структурная составляющая — ледебурит. Это эвтектика, т. е. равномерная механическая смесь зерен аустенита и цементита, получающаяся в процессе кристаллизации. Ледебурит содержит 4,3% углерода. Он образуется при температуре 1147°С. Первоначальная структура его не сохраняется при температурах ниже 727 °С, так как содержащийся в нем аустенит при 727 °С превращается в перлит. При температурах ниже 727 °С (вплоть до комнатной) ледебурит представляет собой механическую смесь перлита и цементита. Ледебурит отличается большой твердостью (550 НВ) и хрупкостью.
Изучение структурных составляющих железоуглеродистых сплавов позволяет сделать следующий важный вывод — при комнатной температуре железоуглеродистые сплавы всегда состоят из двух структурных элементов: мягкого пластичного феррита и твердого цементита, упрочняющего сплав. Эти элементы могут образовать механическую смесь либо находиться в свободном состоянии.
2.2 Диаграмма состоянияжелезоуглеродистых сплавов
Русский металлург, ученый Д.К. Чернов опубликовал в 1868 г. ряд работ, связанных с объяснениями процессов, протекающих в железоуглеродистых сплавах при их нагревании до жидкого состояния и охлаждении. Для объяснения этих процессов он предложил диаграмму «железо — углерод», которая графически изображает состояние сплава железа с углеродом при различных температурах в условиях равновесия.
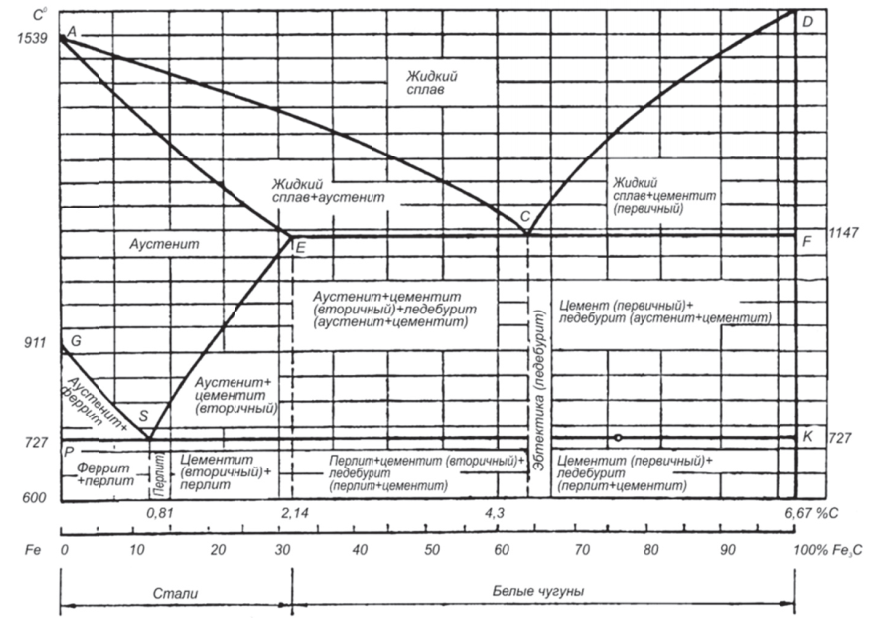
Рис. 10. Диаграмма состояния «железо — углерод»
Диаграмма состояния железоуглеродистых сплавов представлена на рис. 10. Она охватывает не все сплавы железа с углеродом, а лишь те, которые содержат до 6,67% углерода, что соответствует весовому процентному содержанию углерода в карбиде железа — Fe3C. Это объясняется тем, что железоуглеродистые сплавы, содержащие более 5% углерода, не представляют практического интереса. Содержание углерода 6,67% взято в качестве предела на том основании, что при таком его количестве образуется химическое соединение Fe3C (цементит), которое может рассматриваться как самостоятельный компонент сплава.
Диаграмма условно разделена на две части: диаграмму углеродистых сталей и диаграмму белых чугунов.
Углеродистые стали — это сплавы железа, содержащие до 2,14% углерода. Стали, имеющие в своем составе до 0,8% углерода, называются доэвтектоидными, 0,8% углерода — эвтектоидными, свыше 0′,8% углерода (до 2,14%)- заэвтектоидными.
Белые чугуны — это сплавы железа, содержащие от 2,14 до 6,67% углерода. При содержании от 2,14 до 4,3% углерода белые чугуны называются доэвтектическими, при 4,3% — эвтектическими и при 4,3-6,67% — заэвтектическими.
На диаграмме (рис. 10) показано состояние сплавов при первичной и вторичной кристаллизации.
Процессы первичной кристаллизации характеризуются кривыми ACD и AECF.
Кривая ACD отображает температуры, при которых начинается затвердевание железоуглеродистых сплавов. Кривая AECF соответствует температурам, при которых процесс кристаллизации заканчивается. Линия АЕ относится к сталям, а линия ACF — к белым чугунам. Точка А характеризует температуру плавления чистого железа (1539°С), а точка D — температуру плавления цементита — Fe3C (~ 1600°С). Точка Е соответствует максимальному количеству углерода, которое может быть растворено в аустените при высоких температурах. Точка С указывает на состав эвтектики, она соответствует содержанию в сплаве 4,3% углерода. Температура образования эвтектики 1147°С. Линия ECF называется эвтектической, так как в любой ее точке происходит образование эвтектики (ледебурита).
В процессе первичной кристаллизации, по линии АС, из жидкого сплава будут выделяться кристаллы твердого раствора углерода в железе, т. е. аустенит. При содержании углерода в сплавах до 2,14% (углеродистые стали) первичная кристаллизация закончится образованием однородного по составу аустенита. Для сплавов с содержанием углерода от 2,14 до 4,3% (доэвтектические чугуны) первичная кристаллизация закончится образованием аустенита, при понижении температуры на линии ЕС образуется эвтектика, содержащая 4,3% углерода, т. е. ледебурит, и вторичный цементит, который выделится из перенасыщенного углеродом аустенита при температурах ниже 1147°С — в процессе вторичной кристаллизации. В точке С при 1147°С образуется эвтектика, содержащая 4,3% углерода, т. е. ледебурит.
На линии CF (заэвтектические чугуны) из жидкого сплава выделится тот компонент, который является избыточным по отношению к эвтектике, т. е. цементит (в эвтектике содержится 4,3% углерода, а в цементите- 6,67%). Так как цементит образуется при первичной кристаллизации, его называют первичным. На линии CF возникнет эвтектика — ледебурит. Следовательно, в результате первичной кристаллизации заэвтектические чугуны будут состоять из первичного цементита и ледебурита. Линия ECF (1147°С) называется эвтектической, так как на ней происходит образование механической смеси аустенита и цементита — ледебурита. Ледебурит имеет эвтектический состав, следовательно, его кристаллизация протекает при постоянной температуре 1147°С.
В результате первичной кристаллизации сталь получает структуру аустенита, характеризующуюся хорошей пластичностью и вязкостью. Поэтому такая сталь хорошо поддается обработке давлением при высоких температурах. Белые чугуны имеют в своем составе хрупкий и твердый ледебурит, который исключает возможность их обработки давлением даже при высоких температурах. Эта разница в технологических свойствах железоуглеродистых сплавов делает содержание углерода 2,14% той границей между сталью и белыми чугунами, за которой при первичной кристаллизации появляется ледебурит.
Процессы вторичной кристаллизации стали. Если бы железо не испытывало структурных превращений в твердом состоянии, то диаграмма состояния железоуглеродистых сплавов при всех температурах ниже !147°С (вплоть до комнатной) была бы одинаковой (рис. 10, линия AECF). Однако железо подвержено аллотропическим превращениям, поэтому эти сплавы не сохраняют своей первичной структуры.
Рассмотрим процессы вторичной кристаллизации сталей. Для наглядности выделим левую часть диаграммы (рис. 10), охватывающую процессы вторичной кристаллизации стали (рис. 11).
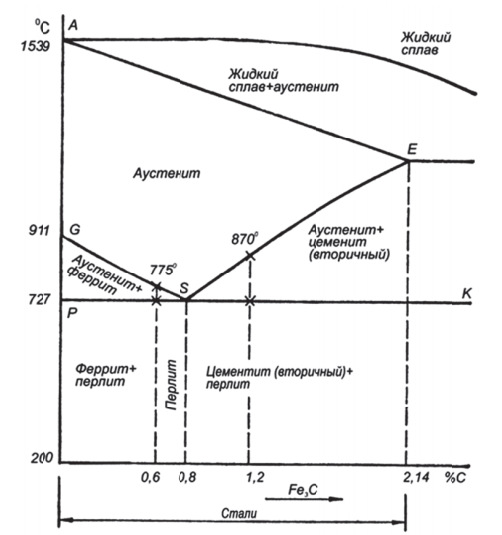
Рис. 11. Область сталей диаграммы состояния «железо — углерод»
Первичная структура стали включает зерна аустенита. Она сохраняется до линии GSE (рис. 10 и 5.11). Указанная линия соответствует температурам, при которых начинается вторичная кристаллизация сталей различного состава. Линия PSK характеризует температуру, при которой завершаются процессы вторичной кристаллизации. Для сталей, представленных на диаграмме, эта температура равна 727°С. При температурах ниже 727°С существенных превращений в сталях не наблюдается, структура, полученная при 727°С, сохраняется при дальнейшем охлаждении сплава (вплоть до комнатной температуры). Линия PSK называется эвтектоидной. Точка S диаграммы соответствует составу эвтектоида — перлиту.
В чем заключаются структурные превращения, которые происходят со сталью в твердом состоянии? Точка G соответствует превращениям, происходящим в чистом железе при 911°С (рис. 11).
Линия GS диаграммы отражает температуры для сталей, содержащих до 0,8% углерода, соответствует температурам, при которых начинается выделение феррита из аустенита. Рассмотрим подробнее, как будет протекать процесс вторичной кристаллизации стали, содержащей 0,6% углерода. Указанная сталь сохраняет первичную структуру аустенита до температуры 775 °С. При этой температуре начинается ее аллотропическое превращение, т. е. выделение феррита из аустенита. Так как в феррите содержится ничтожное количество углерода, оставшийся аустенит будет постепенно, по мере выделения феррита, обогащаться углеродом. Когда концентрация углерода в оставшемся аустените достигнет 0,8%, при 727 °С произойдет распад аустенита на равномерную механическую смесь феррита и цементита, которая называется перлитом. Таким образом, в интервале температур от 775 до 727°С сталь, содержащая 0,6% углерода, будет иметь в своем составе феррит и аустенит, а при температурах ниже 727°С — феррит и перлит. Структура феррит — перлит сохранится без значительных изменений и при дальнейшем охлаждении стали вплоть до комнатной температуры. Аналогичные превращения характерны для всех доэвтектоидных сталей (содержащих менее 0,8% углерода). Разница будет лишь в температуре начала выделения феррита.
Если сталь содержит 0,8% углерода, ее вторичная кристаллизация будет протекать при постоянной температуре (727°С) и сопровождаться только одним процессом- образованием перлита.
Это объясняется тем, что в данном случае содержание углерода в стали соответствует эвтектоидному составу. Процесс вторичной кристаллизации стали, содержащей более 0,8% углерода, характеризуется линиями SE и SK (рис. 11). Точка Е указывает на максимальное количество углерода, которое может быть растворено в аустените, а точка S — на количество углерода, которое может быть растворено в аустените при 727°С. Линия ES соответствует предельной растворимости углерода в аустените при различных температурах. На линии SK заканчивается вторичная кристаллизация сталей, имеющих в своем составе более 0,8% углерода, с образованием перлита (в результате распада аустенита).
Как происходят процессы вторичной кристаллизации стали, содержащей 1,2% углерода? Сталь с таким количеством углерода сохраняет первичную структуру аустенита при охлаждении до 870°С. При более низкой температуре аустенит не способен растворить 1,2% углерода, поэтому при дальнейшем охлаждении сплава из кристаллической решетки аустенита будет выделяться избыточный углерод в виде цементита. Так как этот цементит образуется в результате вторичной кристаллизации, его называют вторичным цементитом и обозначают Fe3Cn. Вследствие выделения цементита содержание углерода в оставшемся аустените будет непрерывно снижаться и при температуре 727°С достигнет 0,8%. При этой температуре аустенит превратится в перлит. На этом процесс вторичной кристаллизации закончится.
Таким образом, рассматриваемая сталь в интервале температур от 870 до 727°С имеет структуру аустенита и вторичного цементита, а при температурах ниже 727°С состоит из вторичного цементита и перлита. Аналогичные превращения в твердом состоянии испытывают все заэвтектоидные стали, т. е. стали, содержащие более 0,8% углерода, разница между ними лишь в температурах начала выделения вторичного цементита.
В структуру доэвтектоидных сталей при комнатной температуре входят феррит и перлит. Чем больше в них углерода, тем больше будет перлита и меньше феррита. Эвтектоидная сталь содержит только перлит. Структура заэвтектоидиых сталей при комнатной температуре — перлитоцементитная. С увеличением в этих сталях углерода растет количество цементита и уменьшается количество перлита.

