Содержание страницы
Технология переработки кино-, фото- и рентгеновских плёнок
Все фотографические материалы состоят из светочувствительных эмульсионных вспомогательных слоев и подложки. В качестве последней применяются высокополимерные пленки, стекло и бумага. Фотографические эмульсионные слои содержат галогениды серебра в виде дисперсных кристаллов, равномерно распределенных в желатине. Фотоэмульсионный слой в обычных высушенных светочувствительных материалах содержат 40…60 % галогенидов серебра (обычно АgВr), 30…50 % желатина и 6…10 % воды. Содержание галогенидов серебра в фотографических слоях изменяется в очень широких пределах в зависимости от характера, назначения и типа фотоматериалов.
На рис. 46 показано строение фотографических материалов для черно-белой фотографии. Защитный слой 1, представляющий собой пленку хорошо надубленного желатина, толщиной около 1 мкм, который предохраняет эмульсионный слой 2 от возможных механических повреждений, снижает мутность эмульсионного слоя и повышает контрастность материала.
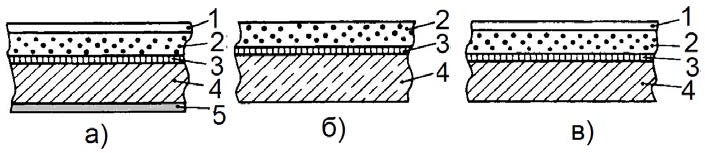
а) – фотографическая пленка; б) – фотографическая пластинка; в) – фотографическая бумага;
1 – защитный слой; 2 – эмульсионный слой; 3 – подслой; 4 – подложка; 5 — противослой
Рисунок 46 – Строение фотографических материалов для черно-белой фотографии
Толщин а эмульсионного слоя в обычных пленках составляет: в негативных 15…25, позитивных 10…15 и бумагах 6…12 мкм (чернобелые) и 25…45 мкм (цветные фотоматериалы). Микрокристаллы состоят в негативных эмульсиях из бромида серебра с примесью иодида и в позитивных – из бромида, бромид-иодида, бромид-хлорида и хлорида серебра.
Подслой 3 служит для прочного сцепления эмульсионного слоя 2 с подложкой 4 из пленок и пластинок. В фотобумаге он, кроме того, предотвращает проникновение эмульсии в подложку. На пленках и пластинках толщина желатинового подслоя около 1 мкм; для фотобумаги в подслой вводят сернокислый барий для повышения ее белизны. Соответственно увеличивается толщина подслоя.
Подложка может состоять из пленки, стекла и бумаги. Фото- и кинопленку в настоящее время обычно изготовляют из триацетатной целлюлозы.
Противослой 5, состоящий из желатина или лака, предохраняет пленку от скручивания. Будучи подкрашен, он предупреждает образование ореола отражения. Лаковый слой предохраняет пленку от светового воздействия разрядов статического электричества, образующегося при трении пленки.
При изготовлении эмульсий исходными являются водожелатиновый раствор галогенидов (бромистого калия КВr, бромистого аммония NН4Вr, йодистого калия КІ, хлористого натрия NaСl и др.) и раствор азотнокислого серебра АgNO3. Для аммиачных эмульсий применяют водно-аммиачный раствор АgNO3, получаемый при добавлении к водному раствору АgNO3 25 %-ного раствора аммиака по суммарной реакции
AgNО3 + 2NН4ОН = [Аg (NН3)2]NO3 + 2Н2O. (7)
При смешении исходных растворов протекают следующие реакции
AgNО3 + МеHaI = АgНаI + МеNO3 (8)
или
[Аg( NН3)2]NO3 + МеНаI = АgНаI + МеNO3 + 2NH3 , (9)
где Ме — К, Na или NН4; NаI — Вr, I или Сl.
Галогенид серебра выделяется из раствора в виде микрокристаллов, равномерно заполняющих желатиновую среду. В 1 см3 эмульсии в зависимости от условий синтеза может присутствовать от 109 до 1014 микрокристаллов.
Полученную эмульсию, точней суспензию, выстаивают, удаляют из нее промывкой или другими способами нитрат того или иного металла, остаточный аммиак и избыточную соль галогена и подвергают второму выстаиванию при 40…50 °С, при котором в кристаллах галогенидов возникают центры светочувствительности. Затем эмульсию охлаждают до превращения в твердый студень. При изготовлении фотографических материалов этот студень расплавляют, фильтруют эмульсию, наносят ее на подложку в поливных машинах, а нанесенные эмульсионные слои подвергают студенению и сушке.
В фотоэмульсию помимо основных реагентов вводят: стабилизаторы, сохраняющие свойства эмульсии длительное время, пластификаторы, придающие гибкость и пластичность желатиновому слою, дубители, повышающие точку плавления и прочность желатинового слоя, антисептики, предохраняющие эмульсию от воздействия бактерий.
При экспонировании фотографического слоя в освещенных его местах происходит фотохимическая реакция, при которой в кристаллической решетке галогенида (бромида) серебра электроны переходят от ионов галоида (брома) к иону серебра
![]() (10)
(10)
где hγ — энергия кванта.
Образовавшийся по этой реакции бром, покидая микрокристалл, поглощается желатиной эмульсионного слоя. Выделяющееся серебро служит для образования скрытого фотографического изображения.
Проявление заключается в обработке пленки медленно действующим органическим восстановителем (гидрохиноном, метолом или другими соединениями), избирательно восстанавливающим серебро в тех зернах АgВr, которые уже содержали его в виде зародышей скрытого изображения.
На примере гидрохинона процесс протекает по схеме:
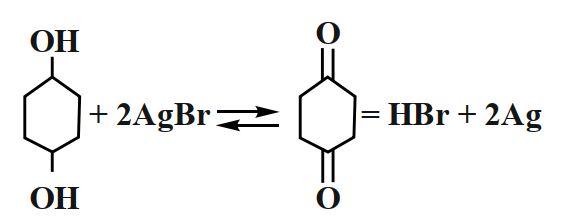 (11)
(11)
В результате скрытое изображение усиливается и становится видимым серебряным изображением. Это изображение является обратным — негативом, на котором светлым областям оригинала соответствуют темные пятна и наоборот.
Целью последующей за проявлением операции фиксирования является полное удаление из эмульсионного слоя не восстановленного при проявлении галогенида серебра. Для его растворения используют вещества, образующие с серебром растворимые комплексные соединения. Наиболее широкое применение для фиксирования приобрел тиосульфат натрия, кристаллогидрат которого именуется гипосульфитом. Кроме тиосульфата натрия в качестве фиксирующего вещества используют тиосульфат аммония.
Растворимости галоидных солей серебра в воде очень малы.
Произведение растворимости бромистого серебра
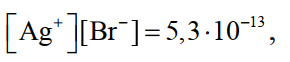 (12)
(12)
т.е. при растворении АgВr в чистой воде насыщение наступает при концентрации серебра ≈ 8…10-5 г/л. Концентрацию насыщения при данном значении произведения растворимости можно увеличить,
уменьшая диссоциацию серебряной соли в растворе. Это достигается
растворением бромистого серебра в растворителях, дающих с серебром комплексные соединения. Если комплексный ион, содержащий серебро, диссоциирует в растворе по уравнению
![]() (13)
(13)
то константа диссоциации
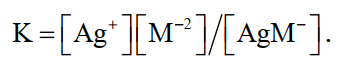 (14)
(14)
Чем меньше константа диссоциации комплексного иона серебра, тем больше в растворе должна быть общая концентрация серебра, т.е. тем более растворим галогенид серебра, в данном случае АgВr.
В литературе приводятся различные формулы комплексных соединений серебра, которые в общем виде могут быть представлены формулой
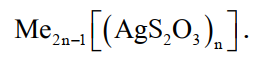 (15)
(15)
Константы диссоциации комплексных ионов
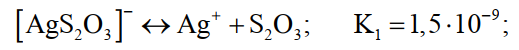 (16)
(16)
![]() (17)
(17)
![]() (18)
(18)
При избытке тиосульфата в реальных растворах для обеспечения надлежащего качества фотографий при фиксировании применяют примерно 10-кратное количество тиосульфата по сравнению со стехиометрическим необходимым) в растворе присутствуют одновременно все три комплексных иона, причем преобладают ионы-5. С поправкой на указанный выше состав комплексного иона в фиксажном растворе, существует следующая система равновесий
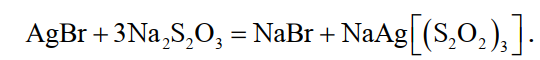 (19)
(19)
При увеличении количества растворенного серебра растет концентрация соли Na5[Аg(S2O3)3], концентрация комплексного иона-5 и, следовательно, концентрация Аg+. Когда последняя увеличивается настолько, что будет достигнуто произведение растворимости АgВr, раствор будет насыщен бромистым серебром. Применение избытка тиосульфата обеспечивает полный переход бромистого серебра в раствор. Обычно исходные фиксажные растворы содержат 250…400 г/л пятиводного тиосульфата натрия.
Содержание серебра в черно-белом изображении зависит от сюжета объекта съемки и других факторов. На построение изображения расходуется меньшая часть серебра из эмульсионного слоя, большая же его часть переходит в фиксажный раствор. В среднем в фиксажный раствор переходит 50…60 % серебра от нанесенного на светочувствительные материалы. В случае фиксирования фотопластинок и фотобумаги этот показатель может достигать 75 %, при фиксировании же цветных пленок, фотопластинок со снимками спектральных линий, пленок с осциллограммами, промышленных и медицинских рентгеновских снимков – 80…90 %.
Отработанные фиксажные растворы, образующиеся у мелких потребителей светочувствительных материалов, обычно содержат 2…7 г/л, редко 14…15 г/л и лишь в исключительных случаях 20 г/л серебра.
В этих растворах всегда имеется большой избыток свободного тиосульфата натрия (или, реже, аммония) и бромистый натрий. В них могут присутствовать добавляемые в процессе фиксирования метабисульфит калия, уксусная кислота, хлористый аммоний, алюминиевые или хромовые квасцы, примеси солей железа, меди и свинца, а также не отмытые компоненты проявителя и продукты его разложения.
Отработанные фиксажные растворы, поступающие на извлечение серебра, весьма неоднородны по составу. Они часто загрязнены посторонними веществами, попадающими в них при транспортировке и в результате смешивания с другими растворами, применяемыми в фотографии, например, при отбеливании, вирирования и т.д. Первые (непроточные) промывные воды от промывки фотоматериалов после фиксирования содержат 1…2 г/л серебра.
На рис. 47 показана схема распределения серебра по продуктам переработки светочувствительных серебросодержащих отходов (на основе усредненных показателей). Баланс показывает, что в отходах фотоматериалов (не считая отходов пленки и бумаги) подлежит возврату около 65 % серебра, нанесенного на светочувствительные материалы.
В состав отходов пленки и фотобумаги входят изношенные («битые») кинофотопленки, потерявшие свое значение негативные и позитивные фотоснимки и рентгеновские снимки, различные обрезки кинофотопленки и фотобумаги, бракованные, засвеченные или потерявшие чувствительность из-за долгого хранения фотоматериалы.
Основными сдатчиками этих отходов являются сеть кинопроката (срок службы демонстрируемого фильма, как правило, не превышает двух лет), рентгеновские кабинеты, фотоателье, лаборатории научных учреждений. Битая пленка образуется также у фотолюбителей, в организациях, занимающихся аэрофотосъемкой и т.п.
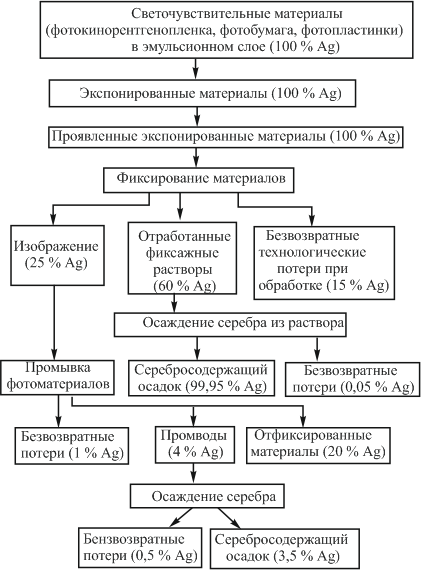
Рисунок 47 – Технологическая схема переработки серебросодержащих светочувствительных отходов
Цветная фотопленка является многослойной. Она содержит три эмульсионных слоя, в которых помимо веществ, применяемых для черно-белого изображения, содержатся компоненты, которые при появлении дадут цветное изображение (красители). В зависимости от состава красителя получается желтое, пурпурное и голубое окрашивание снимка. В результате цветного проявления в отдельных слоях материала образуются однокрасочные и серебряные изображения. Кроме того, в одном из слоев (фильтровом) остается коллоидное серебро. Так как серебряные изображения и фильтровый слой закрывают цветное изображение, серебро следует удалить из материала. Эту операцию производят в две стадии – отбеливанием красной кровяной солью и фиксированием с помощью тиосульфата.
Брак цветной кинофотопленки содержит очень малое количество серебра, а в ряде случаев вообще не содержит его. Вполне очевидно, что нельзя объединить для переработки все поступающие отходы кинофотоматериалов.
С другой стороны, перерабатывать отдельно фотоохоты от каждого сдатчика физически невозможно и нерентабельно, так как встречаются партии отходов массой менее 5 кг, а количество сдатчиков измеряется тысячами. В практике выработана следующая номенклатура перерабатываемых фотоотходов:
- медицинская рентгеновская пленка;
- техническая рентгеновская пленка;
- фотопленка;
- кинопленка;
- фототехническая пленка;
- флюорографическая пленка;
- аэрофотопленка;
- осциллографическая бумага;
- фотобумага.
Длительное время основу кинофотопленки изготовляли из нитроцеллюлозы. Эта пленка была пожаро- и взрывоопасной. Хранение больших количеств такой пленки связано с большим риском. Накопление пленки избегали и ее обычно сразу сжигали. В настоящее время в промышленности используют триацетатную основу пленки, которая не представляет пожарной опасности.
Извлечения серебра из отработанных фиксажных растворов
Сульфидный способ. Важнейшим неметаллическим реагентом для извлечения серебра является сернистый натрий Na2S·9Н2O. Из всех реагентов, предложенных для осаждения серебра, он наиболее доступен, дешев и надежен по полноте и быстроте протекания реакции, которая описывается уравнением
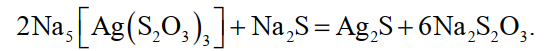 (20)
(20)
Сульфидный способ осаждения серебра основан на малом значении произведения растворимости
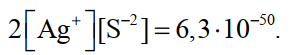 (21)
(21)
Концентрация серебра в насыщенном водном растворе сульфида серебра составляет около 510-15 г/л. В растворе гипосульфита она резко возрастает за счет образования комплексов, но, все же, достигает только величин порядка сотых долей миллиграмма в литре.
Реакция осаждения Ag2S в условиях перемешивания протекает практически мгновенно и до конца. Однако Ag2S выпадает в виде очень тонких частиц, длительность отстаивания которых велика (десятки часов). Скорость отстаивания зависит от дисперсности частиц, которая определяется исходной концентрацией серебра в растворе и зарядом частиц Ag2S. Чем ниже исходная концентрация серебра, тем дисперсией частицы Ag2S и тем медленнее идет отстаивание. При избытке ионов серы или серебра они адсорбируются частицами Ag2S;
взаимное электростатическое отталкивание частиц затрудняет их коагуляцию и ухудшает отстаивание. Отстаивание Ag2S происходит быстрей всего, когда осаждение производилось стехиометрических необходимым количеством Na2S. Скорость отстаивания увеличивается в несколько раз при повышении температуры до 70…80 °С. Расход технического сернистого натрия составляет 1,1 г на 1 г серебра в растворе.
К недостаткам способа относятся:
- медленное отстаивание пульпы и обусловленная этим потребность в больших емкостях, особенно при извлечении серебра из первых промывных вод;
- почти неизбежная грязь при проведении процесса, обусловленная расплыванием сернистого натрия на воздухе;
- выделение сероводорода, требует обязательной установки вентиляции в помещении.
Гидросульфитный способ. Гидросульфит натрия представляет собой кристаллогидрат Na2S2O42Н2O. Осаждение серебра гидросульфитом натрия протекает по реакциям
![]() (22)
(22)
![]() (23)
(23)
Реакции протекают медленней, чем при сульфидном способе и требуют подогрева и перемешивания. Серебро осаждается из растворов полностью. Осадок состоит из смеси металлического и сернистого серебра с содержанием до 80 % Аg. Для осаждения 1г серебра требуется до 6 г технического гидросульфита.
Основное преимущество этого способа заключается в образовании более компактного и легко фильтруемого осадка.
Недостатки способа необходимость подогрева раствора до температуры выше 40 °С, высокая стоимость и значительный расход реагента. Если технический гидросульфит не упакован в герметичную тару, то он окисляется кислородом воздуха и теряет активность. Кроме того, при осаждении серебра выделяется заметное количество токсичного сернистого газа.
Осаждение серебра формалином. Формалин (НСОН) применяется в виде 40 % раствора. Он в обычных условиях не разлагается и полностью осаждает серебро из фиксажных растворов. Однако удельный расход формалина значительно больше, чем расход других применяемых для осаждения серебра реагентов. Существенным недостатком этого способа является неприятный запах в рабочем помещении, что требует усиленной вентиляции. Для организации этого производства требуется согласие санитарно-эпидемиологической станции.
Осаждение серебра ронгалитом. Ронгалит представляет собой формальдегид-сульфоксилат натрия СН2NaНSO32Н2O. При осаждении к фиксажному раствору добавляют ронгалит в тонком порошке в количестве 1,7 г на 1 г серебра. Серебро выделяется в виде металла на стенке реактора. После каждой операции приходится сдирать его с поверхности стенки; при этом возможны потери серебра.
К недостаткам этого способа относится также необходимость организации режима, обеспечивающего сохранность металлического серебра.
Зарубежными патентами предусматривается еще ряд способов извлечения серебра из отработанных фиксажных растворов, например, обработкой их хлором, поваренной солью, йодистым калием, гидролизованным раствором сахара или отработанным проявителем. Тиосульфатных раствор можно также разложить кипячением с выделением сульфида серебра или упариванием с последующей обработкой концентрированной азотной кислотой.
Выбор химического способа осаждения серебра определяется местными условиями, в первую очередь, доступностью реагентов.
Наибольшее распространение из химических способов в лабораториях и централизованных пунктах получил сульфидный способ.
Восстановление серебра металлами. Способ цементации серебра из фиксажных растворов более электроотрицательными металлами привлекателен тем, что он лишен недостатков, присущих описанным выше химическим способам, — реагенты дешевы, недефицитны и не выделяют вредных газов. В качестве восстановителей используют алюминий, железо и цинк. Исследования зависимости скорости цементации от различных факторов проводились в укрупненном (до 100 л раствора) масштабе. Как правило, растворы характеризуются слабощелочной, реже слабокислой, реакцией.
Опыты с использованием железной стружки — наиболее доступного и дешевого реагента не дали достаточного эффекта; восстановление серебра прекращалось в течение 1 час вследствие образования на поверхности стружки пленок оксидов и серебра, препятствовавших дальнейшей цементации. Последующие опыты проводились только с алюминием (стружка) и цинком (порошок с частицами крупностью ~100 мкм).
На рис. 48 показано влияние величины поверхности алюминия на скорость цементации. Это влияние вполне очевидно.
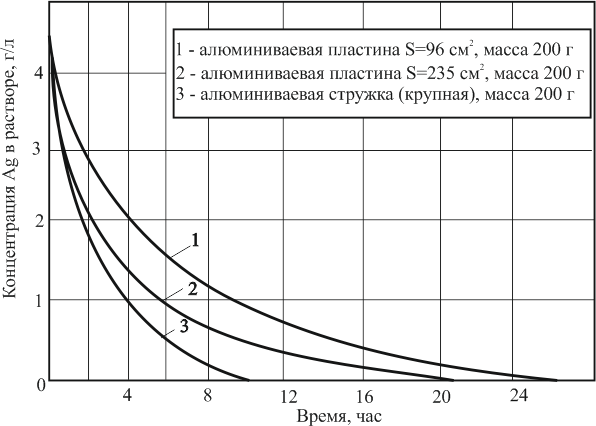
Рисунок 48 – Влияние величины поверхности алюминия на скорость цементации серебра.
При определении удельного расхода металлов-восстановителей оказалось, что он значительно превышает теоретически необходимое количество. Так, в соответствии с уравнениями реакций, теоретический расход алюминия и цинка равен соответственно
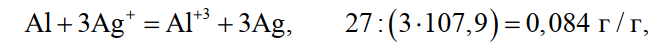 (24)
(24)
![]() (25)
(25)
а фактически он составляет 1,5…2,0 г/г. Сухой шлам от цементации растворов алюминием содержит 58…60 %, а от цементации цинком 40…50 % серебра. Наиболее эффективным и удобным восстановителем является цинковая пыль. Оптимальные условия цементации: температура 18…20 °С и кислотность раствора, не превышающая 0,05 %. Перед осаждением серебра необходимо определить его содержание в отработанных фиксажных растворах и установить дозировку осаждающего реагента. На рис. 49 показана технологическая схема извлечения серебра из отработанных фиксажных растворов сульфидным способом.
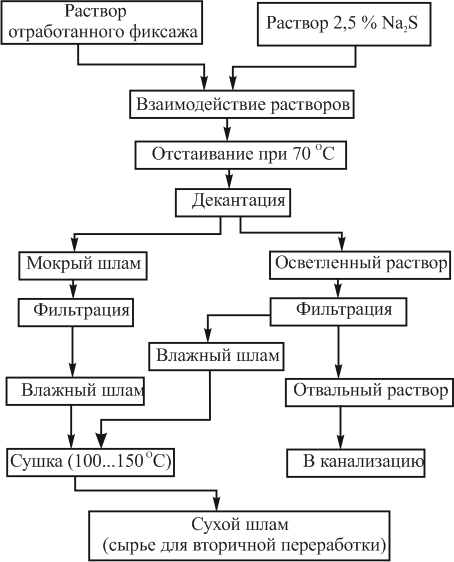
Рисунок 49 – Технологическая схема извлечения серебра из фиксажных растворов
Полное осаждение происходит за 20…24 час. Конец осаждения определяется по отсутствию черного осадка в пробирке с пробой, обработанной сернистым натрием.
Ионообменный способ. В современной металлургии драгоценных металлов ионный обмен применяется для извлечения золота и серебра из цианистых и аммиачных растворов, получаемых при переработке руд и концентратов, содержащих эти металлы.
При переработке фиксажных растворов этот способ еще не приобрел промышленного значения, хотя многочисленные исследования, проведенные в нашей стране и за рубежом, свидетельствуют о его перспективности. Для извлечения серебра из фиксажных растворов за рубежом применяются в основном сильноосновные аниониты типа Дауэкс-1 (фирма Dow Chemical, США), поглощающие тиосульфатных комплексы серебра без разложения. Эти комплексы полностью извлекаются при элюировании 6 %-ным раствором NaCl.
При высокой концентрации серебра в растворах этот способ нерентабелен из-за большого расхода дорогих смол и трудности их регенерации. Однако он может быть широко использован для улавливания серебра, присутствующего в небольших концентрациях в промывных водах и растворах, содержащих серебро порядка 0,003…0,005 г/л, сбрасываемых в настоящее время в отвал. В одном из зарубежных патентов предполагается извлекать серебро из фотографических растворов очень малых концентраций обработкой раствора активированным лигнином. Поглощенное им серебро извлекается в виде АgNO3 обработкой лигнина азотной кислотой.
Электролитический способ. Серебро является одним одним из наиболее электроположительных металлов. Стандартный электродный потенциал серебра для реакции Аg → Аg+ + e определяется значением Е0=+0,799 В. В тиосульфатных растворах в связи с комплексообразованием активность ионов серебра снижена, и потенциал серебра смещается в сторону электроотрицательных значений. Но и здесь он остается более электроположительным, чем у большинства металлов.
Для системы
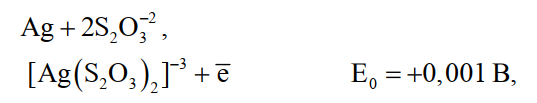 (26)
(26)
а для системы
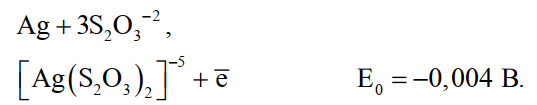 (27)
(27)
При концентрации тиосульфата 250 г/л около 83 % всего содержащегося в растворе серебра находится в виде ионов-5, и зависимость потенциала серебра от концентрации его ионов выражается уравнением Нернста
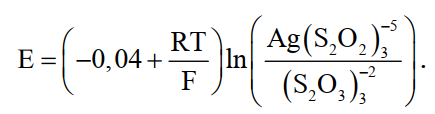 (28)
(28)
В растворе, поступающем на регенерацию с общей концентрацией серебра 2,5…10,0 г/л, потенциал серебряного электрода принимает значение -0,15…0,10 В, а после понижения общей концентрации серебра до 1 мг/л снижается примерно до — 0,34 В.
Выделение серебра на катоде основано, согласно современным воззрениям, на непосредственном разряде комплексного аниона, адсорбированного на катоде, по схеме:
в растворе
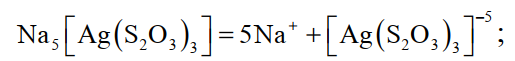 (29)
(29)
в двойном электрическом слое у катода
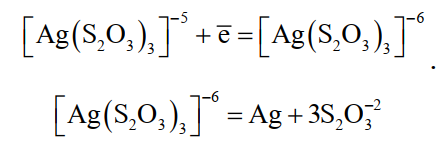 (30)
(30)
В электродных процессах принимают участие только те ионы, которые находятся на расстоянии ионного радиуса от поверхности электрода. По мере снижения концентрации серебра в общем объеме раствора диффузия его ионов к катоду замедляется, концентрация их в пригородном слое резко уменьшается, а это ведет к росту катодной поляризации. В этих условиях становится возможным протекание на катоде побочного процесса восстановления тиосульфатных ионов до сульфидных
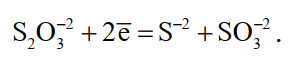 (31)
(31)
Конвективные потоки приводят к смешению католита с раствором в общем объеме ванны, в результате чего происходит осаждение сульфида серебра по реакции
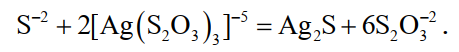 (32)
(32)
Рост катодной поляризации при уменьшении концентрации ионов серебра у катода приводит к выделению на катоде серебра в виде порошка. При этом оба катодных процесса – образование порошкообразного металлического серебра и его сульфида – протекают одновременно, но по мере повышения поляризации доля выделения сульфида возрастает. Одновременно увеличивается дисперсность металлической фазы и уменьшается сцепление осадка с катодом.
Кроме выделения серебра и образования его сульфида на катоде протекают некоторые побочные реакции, вызывающие непроизводительный расход тока. В первую очередь к ним относится выделение на катоде водорода, наблюдаемое по образованию пены у катода при электролизе фиксажных растворов.
Анодный процесс при электролизе тиосульфатных растворов заключается в окислении тиосульфатных ионов до тетратионатных
![]() (33)
(33)
Возможно также образование в результате этого окисления и других политионатов. Значительная часть этих соединений снова восстанавливается у катода до тиосульфата, что вызывает непроизводительный расход тока.
Относительная скорость и последовательность протекания упомянутых выше катодных процессов, определяющие выход по току, зависят от состава фиксажных растворов, содержания в них серебра, плотности тока и температуры. При всех температурах резкое снижение выхода по току наблюдается при переходе от плотности тока, при которой выделяется компактный осадок серебра, к плотности тока, соответствующей выделению шламообразного осадка. Повышение температуры во всех случаях приводит к увеличению выхода по току, особенно сильно при низких концентрациях серебра в растворе. Особенно резко выражена зависимость выхода по току от содержания серебра в растворе. Низкий выход по току в бедных серебром растворах свидетельствует о значительном расходе тока на побочные процессы, не связанные с выделением серебра.
Электролиз отработанных фиксажных растворов на кинокопировальных фабриках, кино- и телестудиях преследует две цели – извлечение серебра и регенерацию фиксажа для повторного использования. Поэтому извлечение серебра из растворов не должно сопровождаться значительным разрушением тиосульфата или загрязнением электролита посторонними примесями.
Это условие выполнимо только при режимах электролиза, сводящих к минимуму рост катодной поляризации, который, как показывает опыт, неизбежен при уменьшении концентрации серебра в электролите ниже 0,5…1,0 г/л или при работе со значительными плотностями тока. Поэтому на предприятиях кинопромышленности при электролизе фиксажных растворов применяют катодную плотность тока в пределах 10…40 А/м2 и извлечение серебра производят не полностью, а лишь снижая концентрацию его до 0,5…1,0 г/л. После этого состав раствора корректируют путем добавления свежего тиосульфата, бисульфата и других компонентов и снова направляют в баки для фиксирования кинопленки. Таким образом, раствор многократно оборачивается в замкнутом цикле. Часть раствора выводится из оборота, так как накопление в нем различных примесей, не удаляемых при электролизе вместе с серебром, ухудшает качество фиксирования. Из этой части серебро извлекают полностью любым из известных способов.
Плотность тока при электролизе зависит от состава отработанного фиксажного раствора и составляет, А/м2: кислый раствор тиосульфата аммония 21,5…43,0; кислый раствор тиосульфата натрия 10,8…21,5; щелочной раствор тиосульфата аммония 10,8…21,5; щелочной раствор тиосульфата натрия 5,4…10,8.
Раствор перемешивают с помощью мешалок, вращающихся между неподвижными электродами, вращающихся катодов, принудительной циркуляции электролита и продувки воздуха.
Кроме энергичного перемешивания в качестве необходимых условий электролиза рекомендуется кислая реакция электролита, присутствие в нем бисульфита натрия и желатины (в пределах 0,01…0,001 %), улучшающей характер катодного осадка.
В целом, для системы извлечения серебра из отработанных фиксажных растворов в кинопромышленности характерны крупные масштабы производства при относительно малой производительности электролизеров, стабильность состава перерабатываемых растворов и получение на катоде компактного осадка металлического серебра. Сдирка катодного осадка с катода трудоемка. Строгое соблюдение заданного технологического режима требует непрерывного контроля за ходом процесса и высокой квалификации обслуживающего персонала.
Ранее указывалось, что увеличение катодной поляризации приводит к выделению на катоде серебряного порошка совместно с сульфидом серебра. Это обстоятельство, ограничивающее повышение плотности тока при электролизе фиксажных растворов в кинопромышленности, было использовано для разработки технологии электролиза, пригодной для условий малых лабораторий, для которых получение на катоде компактного осадка серебра совсем не обязательно. Более того, получение шламообразного серебросодержащего продукта, нуждающегося в последующей металлургической переработке, в данном случае предпочтительней для обеспечения сохранности драгоценного металла.
В этих условиях естественно вести электролиз в таком режиме, чтобы весь осадок получался в виде шлама, который самостоятельно удаляется с катода. Для этого необходимо повысить катодную плотность тока, что приводит одновременно к увеличению производительности электролизных ванн. При таком решении отпадает необходимость перемешивания электролита, а также непрерывного контроля плотности тока и содержания серебра в растворе. Достаточно проверять в конце электролиза полноту осаждения серебра. Наконец, взамен трудоемкой операции сдирки катодного осадка применяются операции отстаивания образовавшейся пульпы и фильтрации сгущенного шлама, требующие минимальных усилий.
Условия сцепления с катодом получаемых осадков, их характер и химический состав зависят от концентрации растворов и плотности тока при электролизе.
Для богатых серебром растворов (~14 г/л Аg) изменение характера катодного осадка от плотного, обладающего металлическим блеском, до черного шламообразного происходит в диапазоне плотностей тока 45…60 А/м2. Дальнейшее повышение плотности тока до 200 и даже 500 А/м2 принципиально не влияет на характер осадка, но существенно снижает содержание в нем серебра.
| Плотность тока, А/м2 | 10 | 60,3 | 201 | 500 |
| Содержание серебра, % | 97,3…97,6 | 94,7…95,6 | 90,4…93,0 | 84,3…84,6 |
При содержании серебра в растворах ≈ 6 г/л полная потеря сцепления осадка с поверхностью катода наблюдается при плотности тока 60 А/м2.
По мере снижения количества серебра в растворе начало образования черного шламоподобного осадка смещается в сторону более низких плотностей тока; для растворов, содержащих 1,0…1,75 г/л серебра черный осадок, содержащий 80,0…81,6 % Аg, образуется уже при плотности тока 10 А/м2. С увеличением плотности тока ухудшается фильтруемость шлама.
Одновременно со снижением содержания в осадках серебра увеличивается содержание в них серы. Рациональный состав осадков, рассчитанный по данным химического анализа, показал, что во всех осадках серебро находилось в избытке против состава Аg2S. Это показывает, что при всех плотностях тока и концентрациях серебра в растворах на катоде происходит разряд ионов серебра до металла. Образование сульфида серебра при высоких плотностях тока — процесс, сопутствующий выделению металлического серебра, а не заменяющий его. Для осадков, получаемых при высоких плотностях тока, характерно образование высокодисперсных частиц металлического серебра, близких по размеру к частицам сульфида серебра. Этим объясняется отсутствие сегрегации частиц при отстаивании и фильтровании пульпы.
Зависимость состава катодных осадков от концентрации серебра в растворе при плотностях тока 60 и 200 А/м2 показала, что с уменьшением концентрации серебра в растворе его содержание в осадке убывает почти линейно; содержание серы в осадке при низких концентрациях серебра в растворе возрастает довольно круто: от 2…3 % до ≈ 8 %.
Исследование показало, что применение плотности тока не ниже 60 А/м2 гарантирует получение самопроизвольно сползающих катодных осадков в растворах с любой концентрацией серебра. Для получения же удовлетворительно фильтрующихся осадков плотность тока не должна превышать 210 А/м2. Это целесообразно и для получения более богатых серебром осадков. Поскольку в промышленных условиях осадки не подвергаются промывке, в дисперсных труднофильтруемых пульпах будет оставаться больше раствора, содержащего гипосульфит и другие компоненты отработанного фиксажного раствора, которые при сушке осадка останутся в нем. Это приведет к разубоживанию шламов и трудностям при их дальнейшей переработке.
Повышение температуры препятствует потере сцепления осадка с катодом. При концентрации раствора 13…15 г/л Аg, плотности тока около 60 А/м2 и 20 °С наблюдалась полная потеря сцепления осадка с катодом, а при 40 °С около 0,9 % (по массе) осадка не смывалось с катода. Аналогичные результаты были получены и для растворов с меньшей концентрацией серебра.
Поскольку с повышением плотности тока пропорционально возрастает производительность ванн, целесообразно работать с максимально допустимыми плотностями тока. Обычно их поддерживают в пределах 120…210 А/м2.
В лабораториях, где перерабатываются небольшие объемы растворов, можно, с целью улучшения фильтруемости пульпы, применять и более низкие плотности тока, но непременно выше 60 А/м2.
Как уже указывалось, при повышенных плотностях тока катодные осадки состоят из дисперсных частиц серебра и его сульфида,
которые сравнительно медленно отстаиваются. Применение флокулянтов полиакриламида, алюминиевых квасцов и других для ускорения отстаивания при исследованиях в ряде случаев давало положительные результаты; однако при массовой проверке в условиях малых лабораторий не удавалось добиться воспроизводимости этих результатов. Это объясняется чрезвычайной неоднородностью химического состава отработанных фиксажных растворов и характера осадков. Удачно подобранные составы осадителей и режимы осаждения для пульпы какого-либо одного состава и характера оказывались непригодными для других пульп. Поэтому флокулянты при отстаивании пульп применения не нашли.
Скорость отстаивания существенно увеличивается при повышении температуры вследствие снижения вязкости растворов, интенсификации броуновского движения и роста кристаллов твердой фазы. Поэтому отстаивание пульпы после электролиза следует вести при подогреве. Однако повышение температуры пульпы увеличивает скорость некоторых нежелательных вторичных реакций, например, выделения сероводорода.
Длительный контакт серебросодержащего шлама с раствором, а также с воздухом в процессе отстаивания и фильтрации, вызывает потери серебра за счет его обратного перехода в раствор. В результате концентрация серебра в фильтрате достигает 0,1…0,2 г/л, а иногда и выше.
Для того чтобы объяснить это явление, нужно подробней рассмотреть равновесия в растворе и в пульпе. Частицы сульфида серебра в пульпе взаимодействуют с тиосульфатными ионами по реакции
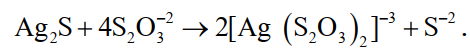 (34)
(34)
Раствор после электролиза содержит окислители – анодные продукты окисления тиосульфата (тетратионат и другие политионаты натрия). Эти анодные продукты окисляют ионы серы по реакции:
![]() (35)
(35)
Поскольку произведение растворимости Аg2S, определяемое как2[S-2], при данной температуре постоянно, исчезновение из раствора ионов серы влечет за собой смещение равновесия реакции вправо, т.е. переход серебра в раствор в составе тиосульфатного комплекса.
Возможно, также непосредственное окисление ионов серы кислородом, растворенным в фиксажном растворе, или кислородом воздуха на границе с раствором.
Наблюдения подтвердили, что скорость обратного перехода серебра в раствор увеличивается в условиях аэрации влажного шлама.
Для сокращения этих потерь серебра необходимо:
- направлять на электролиз фильтрат от фильтрации сгущенного шлама, объем которого составляет 3…5 % от общего объема пульпы;
- максимально сократить продолжительность разделения твердой и жидкой фаз в пульпе.
Электролиз отработанных фиксажных растворов не требует постоянного наблюдения за ходом процесса. Продолжительность цикла электролиза определяется (при полном использовании объема ванны) концентрацией серебра в растворе и силой тока.
В соответствии с законом Фарадея при токе 1 Ампер-час на катоде должно выделиться 107, 9:26,8=4,02 г серебра, где 107,9 — электрохимический эквивалент серебра, а 26,8 — количество Ампер-часов, необходимое для выделения 1 г-экв. любого вещества. Однако по указанным выше причинам выход по току при электролизе отработанных фиксажных растворов составляет около 50 %. Практически можно принять, что 1 Ампер-час выделяет 2 г серебра.
Серебро лучше всего выделяется в слабощелочной среде. Перед началом электролиза рекомендуется добавлять к электролиту техническую кальцинированную соду из расчета 1…2 г соды на 1 л раствора. Это уменьшает выделение сероводорода, увеличивает электропроводность раствора (снижая этим температуру нагрева растворов), повышает катодный выход по току и снижает кислотность растворов, сливаемых в канализацию. Сопоставление электролитических и химических способов извлечения серебра позволяет отметить их достоинства и недостатки.
Общим недостатком химических способов извлечения серебра из отработанных фиксажных растворов является потребность в реагентах, не всегда доступных на местах. Такие реагенты, как гидросульфит и ронгалит дороги и дефицитны. Сернистый натрий — дешевый реагент, но способ с его использованием неудобен из-за длительного отстаивания пульпы. Общим недостатком способов химического осаждения является выделение вредных газов, требующее установки вентиляции и обезвреживания выбросов.
Способы цементации лишены этого недостатка, но они имеют низкую производительность.
Электролитический способ имеет несомненные преимущества перед химическим. Он отличается простотой и не требует расхода реагентов. Электролизные ванны удобны в обслуживании. При электролизе значительно меньше выделяется вредных газов, вызывающих ухудшение санитарно-гигиенических условий труда персонала и загрязнение окружающей среды. Экономические расчеты показали, что применение электролиза обеспечивает самую низкую себестоимость переработки фиксажных растворов, именно по этой причине при организации извлечения серебра из отработанных фиксажных растворов в малых лабораториях предпочтение было отдано электролитическому способу.
Однако местные условия, например, дефицит электроэнергии, очень малые объемы растворов, определяют иногда целесообразность применения химических способов преимущественно осаждения сернистым натрием и цементации. Не исключается и частичное применение осаждения серебра сернистым натрием и в централизованных пунктах-лабораториях, оборудованных электролизными аппаратами.
Извлечение серебра из отходов кино-, фото-, рентгенопленки, фотопластинок и фотобумаги
Процесс сжигания пленки и фотобумаги с последующей металлургической переработкой золы на специализированных заводах не может быть признан принципиально правильным методом извлечения серебра, так как при этом уничтожается основа пленки и фотобумаги. Это противоречит принципу комплексного использования сырья, обеспечивающему максимальный экономический эффект. Однако часто возникают ситуации, когда регенерированная основа пленки и фотобумаги по технологическим причинам не имеет сбыта; в частности, это происходит при переработке смешанного брака пленки. Смешанную регенерированную основу пленки использовать в этом же производстве нецелесообразно, а сортировка ее практически невозможна или обходится очень дорого. В этих случаях некоторые предприятия практикуют способ сжигания пленки и фотобумаги. Однако при реализации этого способа необходимо обеспечить минимальные потери серебра с отходящими газами путем регулирования режима сжигания и надлежащей организации газоочистки. На заводе фирмы «Eastman Kodak» в США сжигание смешанной пленки и фотобумаги производят в специальной печи производительностью 50 т/сут. оборудованной автоматической системой загрузки сырья, колосниковой решеткой с возвратно-поступательным движением для выгрузки золы и вибрационным транспортером, подающим золу непосредственно в бункера. В камере сжигания температуру поддерживают на уровне 760 °С путем регулирования скорости загрузки сырья, подачи первичного воздуха и охлаждающей воды, поступающей в камеру через специальные распылительные форсунки. Горячие газы дожигаются вторичным воздухом в камере дожигания. Отходящие газы орошаются водой в охладительной камере и при 315°С поступают в электрофильтр, улавливающий 99 % пыли. Стоимость печи сжигания и электрофильтра составляет около 1 млн долл., а стоимость извлеченного за год серебра в несколько раз превышает эту цифру.
Однако не все установки для сжигания пленки и фотобумаги характеризуются таким техническим совершенством. В ряде случаев пленку и фотобумагу сжигают в примитивных условиях, при этом теряют часть золы и загрязняют окружающую среду. В настоящее время ведутся исследовательские работы по созданию новых конструкций печей сжигания, обеспечивающих минимальные потери золы.
Исследования, проведенные при сжигании пленки и фотобумаги в печах цеха ВДМ г. Рига (Латвия), показали, что оптимальный выход золы составляет при сжигании всех видов пленки -10 % и при сжигании фотобумаги 18…20 %. Для фотобумаги он выше, поскольку на нее наносят баритовый подслой.
Эти исследования показали также, что при снижении выхода золы из пленки и фотобумаги (за счет увеличения продолжительности цикла сжигания) содержание серебра в золе не возрастает. Очевидно, это происходит из-за улетучивания серебра при длительном нагреве.
При сжигании пленки в печи в описанных условиях не наблюдают так называемого пережога (вкраплений в золе металлических корольков). Эти вкрапления обнаруживаются только в огнеупорных выломках из печи при ее ремонте, которые направляют на специализированный завод для извлечения серебра.
При внепечном сжигании пленки зола часто содержит металлические вкрапления, а общий выход серебра по сравнению с сжиганием в печах, существенно ниже.
В последнее время появились разработки, предусматривающие пиролиз основы пленки и фотобумаги вместо сжигания. При этом, естественно, так же, как и при сжигании, уничтожается основа пленки, но потери серебра могут быть существенно снижены.
Смыв эмульсионного слоя с помощью химических реагентов с неэкспонированной пленки, содержащей серебро в виде бромида, можно проводить кипящей водой. Нарезанную на мелкие куски пленку загружают в бетонные или цементированные баки с водой, нагреваемой острым паром. При этом желатин расплавляется, и эмульсия удаляется с пленки. Однако, желатин удерживает бромистое серебро в суспензии. Для разрушения желатина, после которого бромистое серебро может быть отделено от раствора отстаиванием, эмульсию обрабатывают в бетонных или цементированных баках в течение 3…4 мин кипящим 6 %-ным раствором серной кислоты.
С экспонированной пленки эмульсионный слой смывается с большим трудом. Ее обрабатывают не водой, а горячим раствором каустической соды. При этом кислотная обработка отпадает. Некоторые из предложенных щелочных растворов содержат добавки цианидов, поташа, карбонатной соли и хлористого натрия.
С поверхности фотопластинок – отходов производства и утративших свое значение негативов – эмульсионный слой смывают, погружая их в кипящий (подогреваемый острым паром) разбавленный раствор каустической соды. Длительность обработки составляет 6…8 мин.
В других баках, также при обогреве острым паром, ведут отстаивание, добавляя в качестве коагулянта сульфат алюминия. Отстаивание длится 1,5…2,0 часа, после чего осветленную жидкость декантируют с помощью поплавкового устройства: шлам извлекают из баков по мере накопления. Высушенный в полочных сушильных шкафах шлам содержит до 50 % серебра.
Разработано много вариантов кислотных (с применением соляной, азотной и уксусной кислот) и щелочных способов смыва эмульсионного слоя с фотоотходов. Их общие недостатки: значительный расход химических реагентов, токсичность передела, необходимость оборудования местной вентиляции, необходимость применения флокулянтов для ускорения отстаивания осадка.
В настоящее время чисто химические способы смыва эмульсионного слоя уступают место способам смыва с участием ферментов, подробно описанным ниже.
Эмульсионный слой с поверхности фотобумаги смывают раствором хлорной извести. Обычно для этой цели применяют реакторы из нержавеющей стали вместимостью около 800 л. В реакторе приготовляют 500 л 1,5…2,0 %-ного раствора хлорной извести, загружают в него 120…160 кг отходов фотобумаги и перемешивают механической мешалкой в течение 10…20 мин. При полном удалении эмульсионного слоя глянцевая сторона бумаги становится матовой. Пульпу перекачивают в отстойник из нержавеющей стали. Отстаивание производят в течение 2…4 часа, декантированный раствор фильтруют на нутч-фильтре. Осадок сушат на противнях в полочном электрическом сушильном шкафу при температуре 110…120 °С в течение 24…40 часов, затем охлаждают и упаковывают в металлические ящики.
Отработанную бумагу промывают чистой водой до полного удаления белого хлопьевидного осадка. Промывные воды направляют на отстаивание.
Смыв эмульсионного слоя при участии ферментов. Способ разрушения желатина эмульсионного слоя с помощью ферментов наиболее перспективен. Ферменты — это специфические белковые вещества (с молекулярной массой от десятков тысяч до миллиона и более), служащие биологическими катализаторами. Они способствуют различным превращениям белков, жиров и углеводов, расщеплению или построению их. Как всякие катализаторы, ферменты снижают энергию активации, необходимую для осуществления данной химической реакции, направляя ее обходным путем – через промежуточные реакции, требующие значительно меньшей энергии активации. Активность ферментов очень велика. Они способствуют превращениям такой большой массы вещества, которая во много раз превышает количество самого фермента.
В настоящее время известны более тысячи различных ферментов. Практическое использование в технике, медицине, сельском хозяйстве и других областях находят, главным образом, различные гидролазы-ферменты, катализирующие гидролиз, т.е. расщепление при участии воды различных сложных органических соединений на более простые. Производство ферментных препаратов состоит из двух главных этапов:
- Получение ферментного сырья, т.е. выращивание микроорганизмов (или получение культуральной жидкости), богатых данным ферментом или содержащих фермент специального качества. Реже используют сырье растительного или животного происхождения.
- Выделение из полученного ферментного сырья необходимых ферментных белков либо в виде комплекса, либо отдельных, в той или иной степени очищенных, т.е. выделение ферментов из биомассы микроорганизмов или из соответствующих культуральных жидкостей.
Первый этап является преимущественно задачей микробиологов, второй — биохимиков и химиков белка.
На Шосткинском химическом заводе (г. Шостка, Украина) исследован способ удаления с триацетатной кинопленки фотографической эмульсии и подслоя желатина с помощью бактериальных протеолитических ферментов, содержащихся в культуральной жидкости Bacillus Subtilis-mesentericus. Эта жидкость была получена на полупроизводственной микробиологической установке, построенной на заводе. Измельченную на резательной машине пленку обрабатывали в реакторе при перемешивании раствором фермента при 45 °С. Этот способ обеспечивал регенерацию триацетатной пленки и был внедрен в производство. Количество регенерированной пленки составляло в среднем 250…300 % от неразбавленной культуральной жидкости НБ-8.
Однако активность ферментного раствора была относительно невысокой, что не позволяло достаточно глубоко расщепить желатин. Для получения серебросодержащего шлама пришлось ввести дополнительную операцию кислотного гидролиза эмульсионных смывов.
В институте биохимии НАН Украины разработан способ регенерации серебра и основы триацетатной пленки с помощью препарата Протеназа-1, представляющего собой комплекс протеолитических ферментов, продуцируемый актиномицетом Streptomycins grieses. Этот комплекс, наиболее мощный из всех известных, расщепляет желатин более глубоко, т.е. до наиболее низкомолекулярных фрагментов. Эксперименты показали, что Протеназа-1 интенсивно гидролизует желатин фотоэмульсий, осаждая одновременно с этим шлам, содержащий 45 % серебра (по сравнению с 35 % по старой технологии). Смыв эмульсионного слоя производится при 45 °С. При pH = 6…7,8 гидролиз протекает почти одинаково, что позволяет использовать водные растворы ферментного препарата. Средняя молекулярная масса желатины под действием препарата Streptomycins grieses после 1 часа гидролиза снижалась почти в 20 раз и составляла около 3000, тогда как для молекул исходного белка она равна 60000. За это же время количество серебра в растворе фотоэмульсии падает до нуля. Глубокий гидролиз желатина позволяет смывать с различных видов основы не только эмульсионный слой, но и подслой.
Препарат Протеназа-1 представляет собой сухой порошок, хорошо сохраняющийся и транспортируемый, достаточно стабильный по активности и составу. Применение такого препарата позволило легко регулировать активность и действие ферментного раствора, а также организовать смыв эмульсионного слоя с битой кино-, фото- и рентгеновской пленки непосредственно в местах ее накопления.
На заводе вторичных драгоценных металлов для снятия эмульсионного слоя с пленки предложено применять ферментный препарат Протосубтилин, выращенный из культуральной жидкости продуцента Вас. Subtitles. Этот порошкообразный препарат используется в кожевенной промышленности для смягчения кожсырья и в животноводстве – в качестве добавки к кормам и комбикормам.
Применение ферментов для смыва с пленки эмульсионного слоя практикуется и в зарубежной практике. Так, фирма «Sramес» рекомендует использовать для этой цели панкреатин (трипсин) — протеолитический фермент животного происхождения — и приводит следующий режим смыва эмульсионного слоя с пленки:
- обработка пленки щелочным (рН = 8…9) раствором, содержащим до 0,2 % панкреатина при температуре 40 °С. Расход панкреатина — 1 г/кг рентгеновской пленки;
- разбавление пульпы промывными водами от промывки регенерированной основы пленки;
- подкисление раствора 20 %-ной серной кислотой до рН=2…3, отстаивание, декантация осветленного раствора и сушка серебросодержащего шлама.
Удаление серебра без разрушения основы и желатина. Наибольшее распространение получил способ отбеливания пленок и фотобумаги раствором медного купороса и поваренной соли по реакции
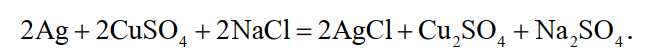 (36)
(36)
Окислительный потенциал системы Сu+2/Сu+ недостаточен для окисления серебра с получением раствора соли серебра ощутимой концентрации. В присутствии NаСl ионы серебра связываются в нерастворимый АgСl, что смещает реакцию вправо. Хлорид серебра откладывается в желатиновом слое пленки. Для его растворения используются фиксажные растворы, часто – сбросные, из которых предварительно электролизом удалено серебро.
Достоинства этого способа – дешевизна и доступность реактивов и вполне приемлемая скорость процесса отбеливания. К недостаткам его относятся многостадийность (отбеливание, обработка фиксажным раствором, извлечение серебра из раствора) и токсичность солей меди.
Этот способ используют также при переработке отходов фотобумаги. Представляет интерес обработка битой (проявленной и отфиксированной) пленки реагентами, окисляющими серебро с образованием его растворимых солей. К таким реагентам относятся персульфат аммония, применяемый в фотографии в качестве ослабителя, сульфат трехвалентного железа и бихромат калия. Наиболее быстро окисляет серебро последний реагент в смеси с серной кислотой (в свежеприготовленном растворе изображение на пленке исчезает в течение 1 мин). Реакция протекает по уравнению
![]() (37)
(37)
Для обработки пленки применяется бихроматный раствор, подкисленный азотной кислотой, взятый с избытком против стехиометрического количества; промывку пленки ведут раствором азотной кислоты при рН = 1,2…1,3. Эти условия обеспечивают получение хорошо растворимого азотнокислого серебра и препятствуют выделению нерастворимого хромата серебра. Серебро из раствора осаждают в виде хлорида насыщенным раствором поваренной соли.
При всех описанных способах обработка пленки производится при комнатной температуре, что исключает необходимость подвода в промышленных условиях пара и электроэнергии и дополнительной вентиляции производственного помещения. Кроме того, работа с горячими растворами ограничивает выбор пластических материалов для изготовления рабочих емкостей. В горячих растворах возможен полный смыв эмульсионного слоя, при котором окисление серебра теряет смысл.

