Содержание страницы
Титан, благодаря своему уникальному комплексу свойств, по праву носит звание «металла будущего». Его история как конструкционного материала началась сравнительно недавно, лишь в середине XX века, что было связано с колоссальными трудностями его получения из рудного сырья. Однако сегодня титан и его сплавы являются незаменимыми в самых высокотехнологичных отраслях. В этой статье мы подробно рассмотрим эволюцию и современное состояние технологий производства порошкового титана — направления, которое открывает новые горизонты для этого удивительного металла.
1. Порошковая металлургия титана: Революция в эффективности
Титан выделяется на фоне других конструкционных металлов благодаря исключительному сочетанию характеристик: низкая плотность (около 4.5 г/см³), высокая прочность, феноменальная коррозионная стойкость и немагнитность. Эти качества сделали его стратегически важным материалом для авиационной, ракетно-космической, судостроительной и химической промышленности. Сплавы титана превосходят большинство сталей и композитов по удельной прочности (отношение прочности к плотности) в широчайшем диапазоне температур: от криогенных (–250 °С) до высоких (+550 °С). По устойчивости к коррозии в агрессивных средах, включая морскую воду, они сопоставимы со сплавами благородных металлов.

В условиях глубокого холода, где многие материалы становятся хрупкими, прочность титана возрастает, а пластичность сохраняется на приемлемом уровне. Это делает его идеальным выбором для криогенной техники, например, для создания резервуаров для сжиженных газов.
Однако технологический путь титана был тернист. Главной проблемой является его высокая химическая активность при нагреве. Уже при температурах 500–750 °С титан начинает активно поглощать кислород и азот из воздуха, становясь хрупким и нетехнологичным. Это явление, известное как геттерный эффект, потребовало создания сложных технологий, где все высокотемпературные операции — от восстановления до плавки и обработки — проводятся в вакууме или в атмосфере инертного газа (аргона). Изначально преимущество отдавалось методам получения компактного металла (слитков), так как они имели меньшую удельную поверхность и, следовательно, меньше загрязнялись примесями.
Несмотря на это, традиционная металлургия титана столкнулась с серьезной экономической проблемой — низким коэффициентом использования металла (КИМ). При механической обработке литых или кованых заготовок в стружку уходит от 60% до 90% дорогостоящего металла. Именно здесь на сцену выходит порошковая металлургия (ПМ), предлагая кардинальное решение этой проблемы. При использовании заготовок, полученных методами ПМ, отходы в стружку сокращаются до 10–25%. Это не только многократно повышает экономическую эффективность, но и расширяет сферы применения титана, делая его доступнее.
Более того, ПМ открывает двери для создания уникальных материалов и изделий, недостижимых для литейных технологий:
- Пористые изделия: фильтры высокой чистоты, имплантаты с биосовместимой пористой структурой.
- Композиционные материалы: дисперсно-упрочненные композиты с повышенной жаропрочностью.
- Специальные покрытия: нанесение износостойких и коррозионно-стойких слоев методом напыления.
- Вспениватели: использование гидрида титана (TiH2) для производства пеноалюминия.
В последние десятилетия, особенно с развитием аддитивных технологий (3D-печати), спрос на качественные титановые порошки многократно возрос. Порошковая металлургия из перспективного направления превращается в одного из ключевых драйверов титановой индустрии, готовясь стать полноценной альтернативой литью во многих традиционных областях.
2. Способы получения титановых порошков: Классификация и особенности
Качество конечного изделия, полученного методом ПМ, напрямую зависит от характеристик исходного порошка: его химической чистоты, формы и размера частиц, насыпной плотности. Поэтому выбор способа производства порошка является определяющим этапом во всей технологической цепочке. Все многообразие методов можно разделить на две большие группы: металлургические и физико-механические.

Металлургические способы предполагают получение порошка непосредственно из титансодержащего сырья (оксидов, хлоридов). Они подразделяются на:
- Металлотермические:
- Восстановление тетрахлорида титана (TiCl4) магнием (процесс Кролля).
- Восстановление тетрахлорида титана (TiCl4) натрием (процесс Хантера).
- Термическая диссоциация иодида титана (процесс Ван Аркеля – де Бура).
- Восстановление диоксида титана (TiO2) кальцием или гидридом кальция.
- Электролитические:
- Электролитическое восстановление соединений титана (оксидов, хлоридов).
- Электролитическое рафинирование титановых отходов или чернового металла в расплавах солей.
Физико-механические способы основаны на переработке уже существующего компактного титана (слитков, губки, отходов) в порошок.
- Механическое измельчение (дробление) кристаллического титана.
- Измельчение предварительно охрупченного титана (например, методом гидрирования-дегидрирования).
- Распыление расплавленного металла инертным газом (газовая атомизация).
- Центробежное распыление расплава с вращающегося электрода или диска.
2.1 Металлотермические методы
2.1.1 Магниетермическое восстановление (Процесс Кролля)
Магниетермическое восстановление тетрахлорида титана — это краеугольный камень современной титановой промышленности. Данная технология является основным способом производства так называемой титановой губки (ТГ) в России, США, Китае и других странах-лидерах отрасли. Качество получаемой губки регламентируется межгосударственным стандартом, например, ГОСТ 17746-96 «Губка титановая. Технические условия».
По своей сути, титановая губка уже является дисперсным материалом, представляя собой спеченный агломерат металлических кристаллов размером от долей до нескольких миллиметров. В традиционном цикле эту губку дробят и переплавляют в слитки в вакуумно-дуговых печах. Однако при дроблении образуется небольшое количество (3–5 %) мелкой фракции (менее 2000 мкм), так называемых «отсевов», которые уже можно считать порошком.
Как показывают данные, представленные в таблице 1, дисперсность губки и выход порошковых фракций можно целенаправленно увеличить, изменяя условия процесса. Например, замена стандартной вакуумной сепарации на гидрометаллургическую обработку (выщелачивание) позволяет получить более мелкокристаллический продукт. Ранее эти возможности не использовались из-за низкого спроса на порошки, но сегодня представляют значительный интерес для оптимизации производства.
Таблица 1. Влияние технологических параметров на дисперсность магниетермической титановой губки
| Источник образца губки | Коэффициент использования Mg, % | Метод выделения из реакционной массы | Физические характеристики дисперсности | |||||
| Удельная поверхность*, м²/г, для фракций, мкм | Пористость, % | |||||||
| Общая | Объем пор <100 нм | |||||||
| до 250 | 250–2000 | 2000–5000 | ||||||
| Блок из промышленного аппарата раздельного типа (3 т) | 60 | Термовакуумная сепарация | 0,21 | 0,31 | 0,19 | – | – | |
| 60 | Термосепарация в потоке аргона | 0,43 | 0,22 | 0,17 | – | – | ||
| 60 | Выщелачивание | 0,61 | 0,48 | 0,38 | – | – | ||
| Промышленный аппарат совмещенного типа (3 т) | Центральный блок губки | 18 | Термовакуумная сепарация | 1,34 | 0,18 | 0,15 | 64,2 | 2,9 |
| «Гарнисаж» (пристеночный слой) | 18 | Термовакуумная сепарация | 0,94 | 0,37 | 0,26 | 55,8 | 4,0 | |
| Центральный блок губки | 60 | Термовакуумная сепарация | 0,23–0,63 | 0,09–0,21 | 0,05–0,18 | 31–46 | 0,6–4,5 | |
| Крупнолабораторный аппарат (20 кг) | 80 | Термовакуумная сепарация | 0,21 | 0,19 | 0,17 | – | – | |
| 80 | Термосепарация в потоке аргона | 0,20 | 0,17 | 0,10 | – | – | ||
| 80 | Выщелачивание | 0,86 | 0,74 | 0,39 | 40,1 | 6,5 | ||
| Продукт диспропорционирования низших хлоридов в расплаве MgCl2 | – | – | 0,34 | 0,51 | 0,18 | 37,6 | 15,2 | |
* Измерено методом тепловой десорбции аргона.
Отсевы дробления губки, как правило, менее пластичны из-за повышенного содержания примесей, но находят применение для напыления покрытий, в самораспространяющемся высокотемпературном синтезе (СВС) карбидов и нитридов, а также в качестве сырья для порошковой металлургии неответственного назначения.
2.1.2 Натриетермическое восстановление (Процесс Хантера)
Натриетермический способ, исторически реализованный в Великобритании и США, предлагает ряд технологических преимуществ перед магниетермическим. Расплавленный натрий легче транспортировать и дозировать, он менее агрессивен по отношению к материалу реактора, а побочный продукт — хлорид натрия (NaCl) — легко удаляется из реакционной массы выщелачиванием водой.
Ключевое отличие этого метода заключается в том, что он позволяет в управляемом режиме получать непосредственно порошковый титан, минуя стадию крупной губки. Варьируя температурный режим, можно получать порошки разной дисперсности. Например, при проведении процесса ниже точки плавления NaCl (801 °С) образуется более тонкий порошок. Обычно свыше 70% частиц имеют игольчатую форму и крупность менее 1000 мкм. При определенных условиях можно получать порошки с размером частиц менее 20 мкм.
На рисунке 1 представлена технологическая схема, разработанная на Березниковском титано-магниевом комбинате (сегодня корпорация «ВСМПО-АВИСМА»), которая демонстрирует промышленную реализацию этого метода.
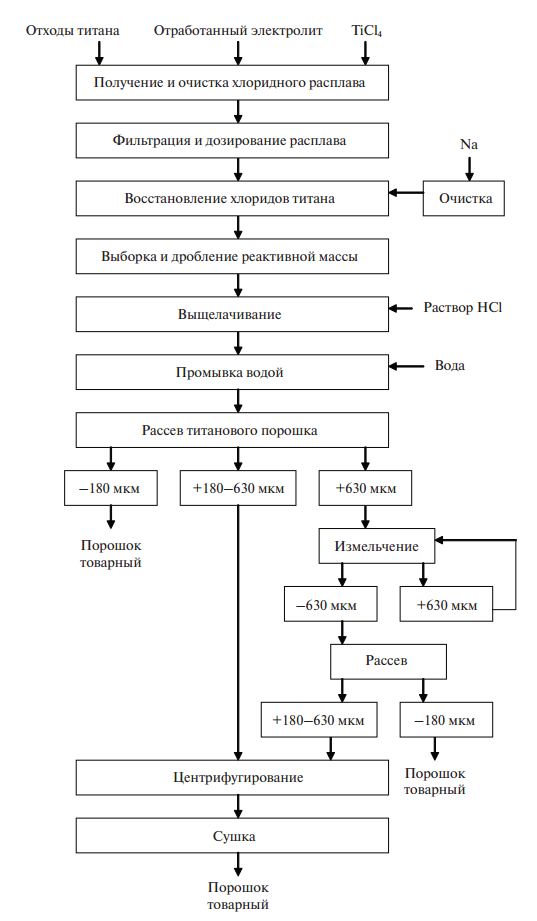
Рисунок 1. Технологическая схема получения порошков титана натриетермическим способом
Процесс может быть реализован в двух вариантах: одностадийном (прямое восстановление TiCl4) и двухстадийном (восстановление из расплава низших хлоридов титана). Двухстадийный вариант, как видно из таблицы 2, позволяет получать более чистый и менее пористый порошок с более высокой пластичностью (меньшей твердостью).
Таблица 2. Сравнительные характеристики натриетермических порошков титана
| Тип процесса | Удельная поверхность фракции 100–500 мкм, м²/г | Пористость, % | Содержание примесей, масс. % | Твердость по Бринеллю, НВ, МПа | |||||
| общая | в т.ч. поры <100 нм | Cl | Fe | N | C | O | |||
| Одностадийный | 1,62 | 29,7 | 1,5 | 0,10–0,15 | 0,01–0,08 | 0,008–0,02 | <0,02 | 0,04–0,3 | – |
| Двухстадийный | 0,38 | 12,5 | 11,2 | 0,10–0,13 | 0,005–0,01 | 0,004–0,008 | 0,003–0,004 | 0,05–0,07 | 1000–1200 |
Несмотря на преимущества, натриетермический способ менее распространен из-за более высокой стоимости натрия по сравнению с магнием. Однако его способность производить порошки заданных характеристик сохраняет его актуальность для нишевых применений.
2.1.3 Термическая диссоциация иодида (Процесс Ван Аркеля – де Бура)
Этот метод является не столько способом массового производства, сколько процессом глубокой очистки (рафинирования) титана. Его суть заключается в так называемой «транспортной реакции». Черновой титан при умеренной температуре (200–400 °С) реагирует с парами йода, образуя летучий тетраиодид титана (TiI4). Газообразный иодид затем разлагается на раскаленной до 1100–1400 °С титановой нити, осаждая на ней кристаллически чистый металл, в то время как высвободившийся йод возвращается в цикл. Этот процесс позволяет получать титан чистотой 99.9% и выше. Хотя в классическом исполнении он дает кристаллические прутки, теоретически, изменив конструкцию зоны диссоциации (например, используя плазменный факел), можно получать и порошок сверхвысокой чистоты.
2.1.4 Восстановление оксида титана кальцием или гидридом кальция
Этот метод привлекателен тем, что позволяет использовать в качестве сырья более дешевый диоксид титана (TiO2) вместо тетрахлорида. Восстановление проводят в атмосфере аргона при 1000–1100 °С по реакции:
TiO2 + 2Ca → Ti + 2CaO
Образующийся оксид кальция (CaO) удаляют выщелачиванием в слабых кислотах. Особенностью процесса является образование высокодисперсного порошка с размером частиц в несколько микрометров. Использование гидрида кальция (CaH2) вместо чистого кальция позволяет проводить процесс более полно и получать на выходе порошок гидрида титана (TiH2), который более устойчив к окислению в ходе последующей гидрометаллургической обработки.
2.2 Электролитические методы
Электрохимические процессы исторически рассматривались как перспективная альтернатива металлотермическим, так как потенциально позволяют создать непрерывное, автоматизированное и менее затратное производство. При электролизе из расплавов солей титан осаждается на катоде в виде дендритных кристаллических осадков, которые после очистки от электролита легко распадаются в порошок.
2.2.1 Восстановление соединений титана
Электролиз диоксида титана. Прямой электролиз TiO2, растворенного в расплавах фтористых или фосфатных солей, является самым коротким путем к получению металла. Однако этот способ имеет серьезный недостаток: сложность полного удаления кислорода из катодного осадка, что приводит к его охрупчиванию. Добиться высокой чистоты металла этим методом пока не удалось.
Электролиз хлоридов титана. Более перспективным является электролиз низших хлоридов титана (TiCl2, TiCl3), растворенных в эвтектических смесях хлоридов щелочных металлов (например, KCl-NaCl). Процесс ведется при 600–750 °С. Этот метод позволяет получать более чистый металл, так как в системе отсутствует кислород. В таблице 3 приведены сравнительные напряжения разложения для различных соединений, иллюстрирующие термодинамическую возможность селективного осаждения титана.
Таблица 3. Теоретическое напряжение разложения некоторых солей
| Соединение | Температура, °С | Напряжение разложения, В |
| NaCl | 877 | 3,35 |
| KCl | 768 | 3,58 |
| MgCl2 | 700 | 2,51 |
| K2TiF6 | 800 | 1,85 |
| TiCl2 | 800 | 1,80 |
| TiCl4 (газ) | 820 | 1,64 |
Регулируя плотность тока, температуру и состав электролита, можно влиять на морфологию и размер частиц катодного осадка, получая порошки с заданными свойствами. Различные варианты процесса представлены в таблице 4.
Таблица 4. Примеры технических параметров для получения порошков титана электролизом
| Состав электролита | Плотность тока, кА/м² | Температура, °С | Ключевые условия и показатели процесса |
| KCl–NaCl–TiCl2 | 5–35 | 780–820 | Время наращивания катодного осадка 2 часа |
| Расплав фторидов NaF/KF | 3–4 | 720 | Электролиз фтортитанатов |
| NaCl–TiCl2 | 1–4 | 850–870 | Выход по току 70–90 %, используется биполярный электрод |
| LiCl–KCl | 25 | 400 | Низкотемпературный процесс, напряжение 2,7 В |
2.2.2 Электролитическое рафинирование
Этот метод является одним из наиболее эффективных для получения высокочистых порошков и, что особенно важно, для переработки отходов и лома титана. Процесс основан на использовании растворимого анода из загрязненного титана или его сплава. В ходе электролиза чистый титан анодно растворяется, переходит через солевой расплав и осаждается на катоде в виде дендритных кристаллов, а большинство примесей (железо, кремний, кислород, углерод) остаются в электролите или оседают в виде анодного шлама.
Этот способ позволяет получать порошки, превосходящие по пластичности и чистоте многие другие типы, что делает их идеальным сырьем для изготовления ответственных конструкционных деталей. Свойства спеченных изделий из такого порошка приближаются к свойствам литого металла марки ВТ1-0. Технология была успешно разработана и внедрена в промышленном масштабе в СССР и до сих пор не имеет полных зарубежных аналогов по эффективности.
2.3 Физико-механические методы
Эти методы не создают новый металл, а лишь изменяют его физическую форму. Они незаменимы для переработки лома, отходов и получения порошков из специфических сплавов.
2.3.1 Метод гидрирования–дегидрирования (HDH)
Способ HDH — один из самых распространенных и универсальных в порошковой металлургии титана. Он основан на обратимом взаимодействии титана с водородом. Процесс включает три стадии:
- Гидрирование: Титановую стружку, губку или лом нагревают в атмосфере чистого водорода при 350–700 °С. Титан активно поглощает водород, образуя хрупкий гидрид титана (TiH2).
- Измельчение: Полученный хрупкий гидрид легко измельчается в шаровых или вихревых мельницах до порошка требуемой фракции.
- Дегидрирование: Порошок гидрида нагревают в вакууме при 700–800 °С. Водород выделяется, оставляя после себя чистый титановый порошок с развитой поверхностью и угловатой формой частиц, идеально подходящей для прессования.
Ключевое преимущество метода — возможность перерабатывать любой вид титанового сырья, включая высоколегированные сплавы, с сохранением их химического состава. Основной недостаток — необходимость контроля остаточного содержания водорода, который может вызывать водородную хрупкость изделий.
2.3.2 Методы распыления расплава (Атомизация)
Методы атомизации — наиболее современные и высокотехнологичные, позволяющие получать порошки сферической формы с превосходной текучестью. Такие порошки являются основным сырьем для аддитивных технологий (SLM, EBM, LMD — 3D-печать).
Газовое распыление (Gas Atomization): Струя расплавленного титана, полученного в индукционной или электронно-лучевой печи, разбивается мощными потоками инертного газа (аргона). Образующиеся капли застывают в полете, формируя сферические частицы.
Центробежное распыление: Этот метод более распространен для активных металлов, как титан. Наиболее известная его реализация — Процесс Вращающегося Электрода (PREP — Plasma Rotating Electrode Process). Вертикально расположенный стержень из титанового сплава вращается с высокой скоростью (до 15 000 об/мин). Его торец оплавляется плазменной дугой, и капли расплава срываются под действием центробежной силы, образуя идеально сферические гранулы с гладкой поверхностью и минимальным количеством сателлитов (налипших мелких частиц). Производительность процесса может достигать 150 кг/ч. Порошки, полученные этим методом, отличаются высочайшей чистотой и идеальной морфологией, что делает их эталонным материалом для аэрокосмической и медицинской отраслей.
Заключение
Промышленность порошкового титана прошла огромный путь развития — от побочного продукта при производстве губки до высокотехнологичного сырья для 3D-принтеров, печатающих детали авиационных двигателей и кастомизированные медицинские имплантаты. Выбор конкретного метода производства сегодня диктуется конечной целью:
- Для недорогих наполнителей и покрытий подойдут отсевы магниетермической губки или порошки, полученные методом HDH.
- Для классической порошковой металлургии (прессование и спекание) оптимальны электролитические порошки и порошки HDH.
- Для аддитивных технологий и наиболее ответственных применений требуются сферические порошки, полученные методами газовой или центробежной атомизации.
Дальнейшее развитие технологий будет направлено на снижение стоимости порошков, повышение их чистоты и создание сплавов с уникальными свойствами, что, несомненно, будет и дальше расширять границы применения «металла будущего».
