Из-за низких механических свойств чистые металлы как конструкционные материалы в машиностроении находят ограниченное применение по сравнению со сплавами.
Сплав — это конструкционный материал, полученный путем сплавления нескольких химических элементов (металлов и неметаллов) и обладающий свойствами, присущими основному сплавляемому элементу.
Металлический сплав может быть получен не только сплавлением химических элементов, но и такими способами, как спекание, электролиз, диффузия, плазменное напыление, возгонка и др. Конструкционный материал, полученный не сплавлением, называется псевдосплавом. Если сплав имеет в своем составе 50 % металла и более, то он называется металлическим сплавом.
Металлический сплав имеет более высокие механические и технологические свойства по сравнению с неметаллическим сплавом. Химические элементы, образующие сплав, называются компонентами.
По своему составу сплавы могут быть двухкомпонентными (металл + металл, металл + неметалл), трех- и более компонентными. Внутреннее строение сплавов определяется формой связи между компонентами.
Двухкомпонентные сплавы при нагревании (охлаждении) в силу особенностей взаимодействия друг с другом ведут себя неадекватно и, в связи с этим, имеют различное физическое строение и свойства.
К промышленным сплавам, которые находят широкое применение, относятся:
- чугун и сталь — сплавы железа с углеродом;
- латунь — сплав меди с цинком;
- бронза — сплав меди с оловом и др.
Сплавы имеют атомно-кристаллическое строение, обладают аллотропией (полиморфизмом) и, по сравнению с чистыми металлами, более высокими механическими и технологическими свойствами.
Форма металлической связи сплавляемых химических элементов влияет на образование структуры сплава, их атомно-кристаллическую решетку.
Фазы. Сплавам, так же как и чистым металлам, характерно атомно-кристаллическое строение. Сплав в твердом состоянии может иметь различную связь атомно-кристаллических решеток. Жидкое или твердое состояние химических компонентов, образующих сплав при определенной температуре и давлении, называется системой.
Однородная часть системы, отделенная от других частей условной границей (линией), называется фазой.
Жидкая фаза характеризуется тем, что атомные кристаллические решетки сплавляемых компонентов распадаются и компоненты растворяются друг в друге или не растворяются и присутствуют в сплаве самостоятельно. Эта закономерность присуща многим сплавам.
Твердая фаза — это однородная часть сплава с определенными атомно-кристаллическим строением и массовой долей сплавляемых компонентов. Атомные решетки сплавляемых компонентов взаимодействуют в строго определенном порядке. Атомные решетки химических элементов, образующих сплав в твердом состоянии, образуют мелкие кристаллы — структуры.
В зависимости от внутреннего строения сплавов и металлической или химической связи между сплавляемыми элементами сплавы подразделяются на две группы:
- однородные сплавы;
- неоднородные сплавы.
Однородные сплавы имеют общие атомные кристаллические решетки, в которые входят атомы сплавляемых компонентов.
Неоднородные сплавы имеют самостоятельные кристаллические решетки сплавляемых компонентов.
По характеру взаимодействия сплавляемых компонентов в твердой фазе различают механические смеси, твердые растворы и химические соединения.
Механическая смесь сплавляемых компонентов А и Б (рис. 1, а) образуется тогда, когда атомные кристаллические решетки сохраняются и не вступают в химическую реакцию с образованием какого-либо нового соединения. Связь между атомными решетками осуществляется за счет металлической связи. Механическая смесь сплава будет неоднородного типа, т. е. сплавляемые компоненты А и Б в сплаве будут самостоятельными и чередоваться между собой в зависимости от их соотношения.
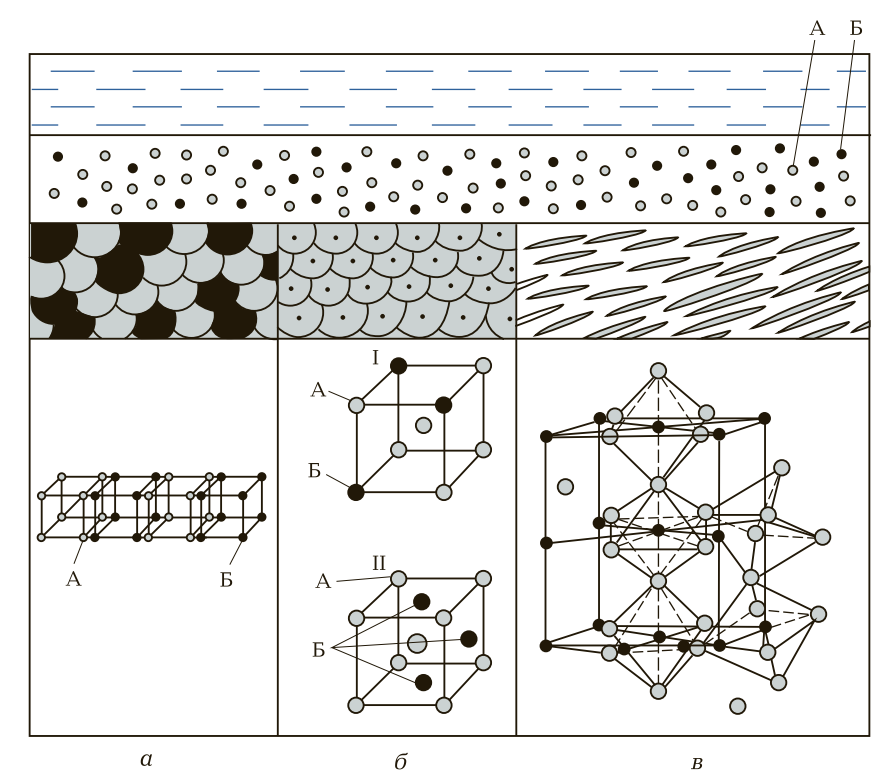
Рис. 1. Схематическое изображение структуры сплава: а — механическая смесь; б — твердый раствор (I — раствор замещения; II — раствор внедрения); в — химическое соединение; А, Б — сплавляемые компоненты
Свойства механической смеси зависят от свойств сплавляемых компонентов А и Б. Как правило, эти микроструктуры имеют относительно высокую твердость, прочность, ударную вязкость, хорошо обрабатываются резанием.
Твердые растворы в зависимости от взаимодействия атомов подразделяются на твердые растворы внедрения и твердые растворы замещения (рис. 1, б ).
На рис. 1, б, I показана атомно-кристаллическая решетка твердого раствора замещения. Атомно-кристаллическая решетка основного компонента А в форме объемно-центрированного куба (девять атомов) сохранилась, но три атома этого компонента замещены атомами сплавляемого компонента Б.
На рис. 1, б, II показана атомно-кристаллическая решетка твердого раствора внедрения. При этом виде образования сплава атомно-кристаллическая решетка основного компонента А сохраняется. Атомно-кристаллическая решетка сплавляемого компонента Б разрушается, и его отдельные атомы внедряются в пространство атомно-кристаллической решетки основного компонента А. Таким образом, в атомно-кристаллической решетке твердого раствора внедрения девять атомов, как в основном компоненте А, плюс два-три атома компонента Б.
Твердые растворы по своим свойствам наиболее близки к свойствам основного компонента. Они имеют низкую твердость, высокую плотность, ударную вязкость, прочность, хорошо деформируются в холодном и горячем состоянии. Микроструктура большинства конструкционных и инструментальных сталей представляет собой твердые растворы внедрения и замещения.
Химические соединения сплава образуются тогда, когда атомно-кристаллические решетки сплавляемых компонентов А и Б распадаются. Отдельные атомы этих компонентов образуют новые атомные решетки, которые по своему типу, форме и числу атомов отличаются от атомно-кристаллических решеток сплавляемых компонентов.
Химические соединения в сплаве образуются при строго определенном массовом соотношении сплавляемых компонентов А и Б. Например, химическое соединение углерода с железом образуется при массовой доле углерода, равной 6,67 %.
Свойства химических соединений также резко отличаются от свойств сплавляемых компонентов. Химические соединения, как правило, очень твердые, хрупкие, тугоплавкие, имеют мелкозернистую или игольчатую микроструктуру. На рис. 1, в показана атомно-кристаллическая ячейка химического соединения углерода с железом. Это сложная ромбическая пространственная атомно-кристаллическая решетка, состоящая из атомов железа и атомов углерода (компонентов А и Б).
В практике чаще всего в сплаве наблюдается смесь нескольких соединений (микроструктур), например механическая смесь химического соединения и твердого раствора или механическая смесь двух твердых растворов.
Диаграммы состояния двухкомпонентных сплавов. Любое изменение химического состава сплава влечет за собой изменение физических параметров: температуры, давления и структуры. Изменение этих параметров на границах фаз происходит скачкообразно или замедленно.
В практике металловедения для определения температур, давления, структуры и взаимодействия сплавляемых компонентов применяют графики — диаграммы состояния сплавов. Для этого нагревают (охлаждают) сплав в закрытом тигле с помощью термопары, по прибору наблюдают поведение этого сплава и по наблюдениям строят соответствующие графики.
На диаграммах состояния отображаются только условия, когда сплав имеет постоянные параметры, — равновесие, поэтому в научной литературе диаграммы состояния также называют диаграммами равновесия. В связи с тем что сплавляемые компоненты (металлы и неметаллы) обладают аллотропией, при нагревании (охлаждении) в сплавах происходят аллотропные изменения. Аллотропные изменения можно наблюдать при лабораторных исследованиях с помощью термического метода, а иногда визуально (цвет сплава становится ярче или, наоборот, тускнеет, или длительное время остается постоянным).
Любое изменение в металле при нагревании (охлаждении) характеризуется определенной температурой, которая называется критической температурой. Критические температуры на прямой отражаются соответствующими точками, которые называются критическими точками. Если рассматривать любой металл или сплав в одном измерении (температура нагрева), то графическая характеристика будет отображена в виде вертикальной прямой, на которой указывают критические температуры (точки). Если состояние металла или сплава рассматривать в двух измерениях (температура нагрева (охлаждения) и время нагрева (охлаждения), то график будет изображен в двух координатах (ось ординат и ось абсцисс).
Для примера рассмотрим состояние чистого железа при нагревании и охлаждении. На рис. 2 приведены критические температуры чистого железа при нагревании (охлаждении). Железо имеет следующие критические точки (температуры): 768; 910; 1 392 и 1 539 °С. При температуре 910 °С Fе-α (α-железо) переходит в Fе-β (β-железо). При температуре 1 392 °С Fе-β переходит в Fe-γ (γ-железо). При температуре 1 539 °С Fe-γ начинает медленно расплавляться с поглощением энергии (температуры).
При всех критических температурах на диаграммах показаны задержки перекристаллизации (горизонтальные участки). При охлаждении железа процесс перекристаллизации происходит в обратном порядке.
Для двухкомпонентных сплавов диаграмма состояния — это графическое изображение состояния сплавов в двух измерениях: температура нагрева (охлаждения) и химический состав сплава (концентрация).
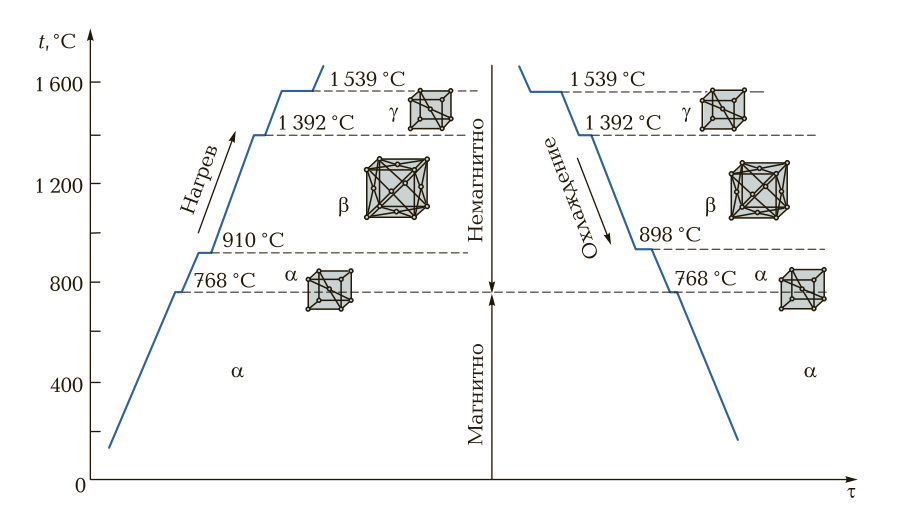
Рис. 2. Кривые нагрева и охлаждения железа: t — температура; τ — время
Температуру нагрева (охлаждения) откладывают по оси ординат, по оси абсцисс откладывают массовую долю сплавляемых компонентов (концентрация).
Для примера рассмотрим диаграмму состояния двухкомпонентного сплава свинец — сурьма (рис. 3). На оси абсцисс слева берем 100 % свинца (Pb), справа — 100 % сурьмы (Sb). Свинец и сурьма в жидком состоянии неограниченно растворяются друг в друге, в твердом состоянии — образуют механическую смесь сплавляемых компонентов.
При нагревании (охлаждении) сплава от твердого состояния до температуры плавления (а при охлаждении от жидкого состояния до температуры затвердевания) в сплаве происходит образование механических смесей (эвтектика) и расплавление при различных температурах.
Возьмем чистый свинец. При нормальной температуре и до температуры 245 °С в свинце никаких изменений внутреннего строения не происходит, и свинец будет иметь структуру Рb-α (α-свинец). При температуре 245 °С Рb-α перестраивается в Рb-β (β-свинец). Эта структура остается до температуры 327 °С.
При температуре 327 °С свинец начинает расплавляться. При расплавлении за счет поглощения энергии (температуры) температура свинца остается постоянной — 327 °С. При охлаждении свинца процесс происходит в обратном порядке.
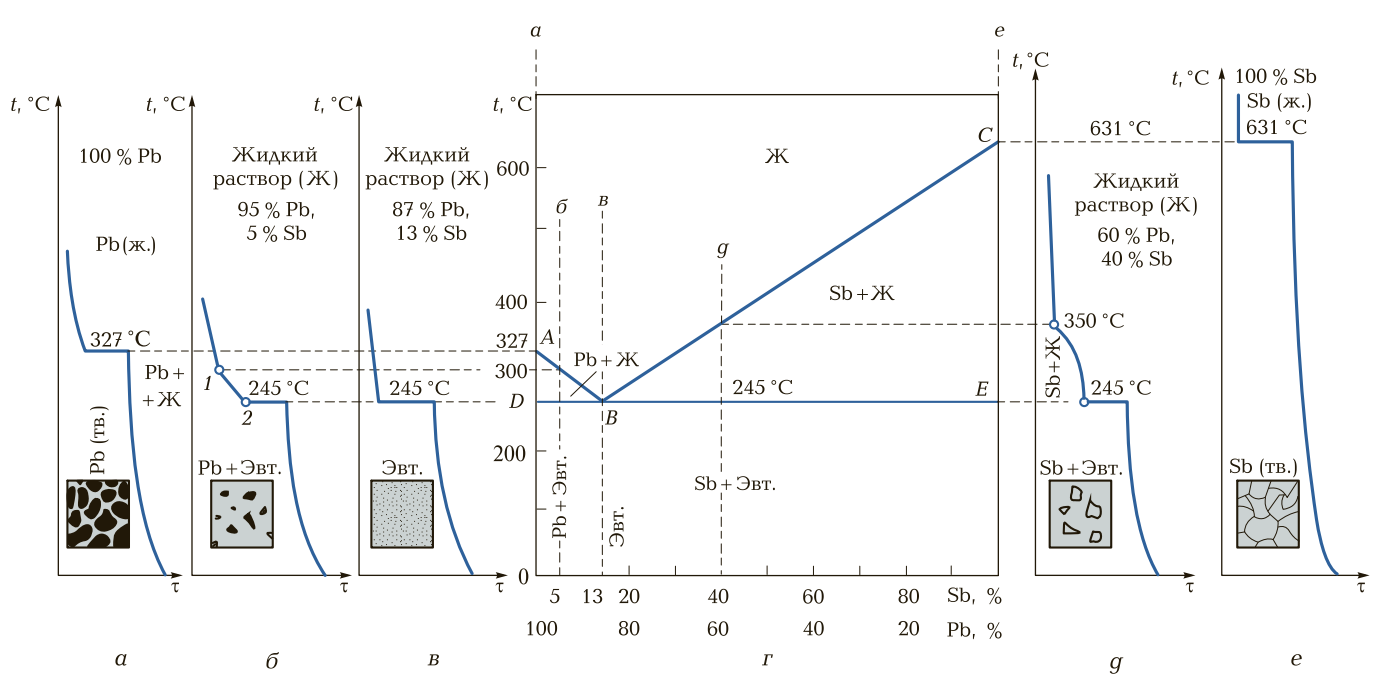
Рис. 3. Кривые охлаждения и структуры (а, б, в, д, е), диаграмма состояния (г) сплавов свинец—сурьма: 1 — температура ликвидуса; 2 — температура солидуса; АВС — линия ликвидуса; DBE — линия солидуса; Ж — жидкость; Эвт. — эвтектика
При нагревании сурьмы до температуры 245 °С никаких изменений в металле не происходит. Структура сурьмы будет Sb-α (α-сурьма). При температуре 245 °С Sb-α переходит в Sb-β. При температуре 631°С сурьма начинает расплавляться. В связи с тем что при расплавлении происходит большое поглощение теплоты, температура расплавления сурьмы на 8 … 10 °С будет ниже. При охлаждении процесс идет в обратном порядке. Далее рассмотрим поведение типовых сплавов свинца и сурьмы: 95 % Рb + 5 % Sb; 87 % Рb + 13 % Sb; 60 % Рb + 40 % Sb. Для составления диаграммы состояния двухкомпонентного сплава свинец — сурьма строим кривые нагрева (охлаждения).
При нагревании (охлаждении) 100 % Pb (рис. 3, а) при температуре 327 °С на графике будет горизонтальный участок. При нагревании (охлаждении) сплава 95 % Рb + 5 % Sb (рис. 3, б) при температуре 245 °С на графике будет горизонтальный участок. Далее при нагревании (охлаждении) при температуре 300 °С будет перегиб кривой, при этой температуре сплав начнет расплавляться (при нагревании) или кристаллизоваться (при охлаждении). При нагревании (охлаждении) сплава 87 % Рb + 13 % Sb (рис. 3, в) при температуре 245 °С также будет горизонтальный участок. При этой температуре сплав начинает плавиться и заканчивает расплавление при температуре 245 °С.
При нагревании (охлаждении) сплава 60 % Рb + 40 % Sb (рис. 3, д) до температуры 245 °С в структуре сплава никаких изменений не происходит. При температуре 245 °С свинец начинает расплавляться — на графике будет горизонтальный участок. При дальнейшем нагревании (охлаждении) при температуре 350 °С сплав расплавляется (при нагревании) или начинает кристаллизоваться (при охлаждении).
При нагревании (охлаждении) 100 % сурьмы (рис. 3, е) до температуры 631 °С сплав будет иметь твердую фазу, и при температуре 631 °С на графике будет горизонтальный участок, сурьма начинает расплавляться. За счет поглощения энергии расплавление сурьмы происходит при температуре несколько ниже 631 °С.
Для наглядного изображения характеристики сплава свинец — сурьма строим следующий график. На оси ординат откладываем температуры нагрева (охлаждения) от нормальной температуры. На этой оси будем откладывать критические точки для 100 % свинца. На оси абсцисс откладываем массовую долю в сплаве свинца и сурьмы. Справа проводим ось температур для 100 % содержания сурьмы. Далее на оси ординат проектируем критические точки, полученные в результате нагрева рассмотренных ранее сплавов.
Как видим из графиков, первое фазовое изменение сплавов происходит при температуре 245 °С. Проводим горизонтальную прямую DE, соответствующую этой температуре. На оси температур свинца проектируем точку, соответствующую температуре 327 °С — температуре плавления чистого свинца. Полученную точку обозначим буквой А.
На оси температур сурьмы проектируем точку, соответствующую 631 °С — температуре плавления сурьмы. Полученную точку обозначим буквой С. На оси абсцисс из точки, соответствующей 87 % Рb и 13 % Sb, восстанавливаем перпендикуляр (пунктиром) до горизонтальной прямой DE (температура расплавления данного сплава). Точку А (критическую температуру 327 °С) на оси ординат соединяем с критической точкой, лежащей на горизонтальной прямой, соответствующей температуре плавления данного сплава (87 % Рb + 13 % Sb). Полученную точку обозначим буквой В.
На оси абсцисс из точки, соответствующей 95 % Рb и 5 % Sb, восстанавливаем перпендикуляр до пересечения с отрезком АВ. В данной точке имеем критическую температуру 300 °С — температуру плавления (затвердевания) сплава 95 % Pb + 5 % Sb.
На оси абсцисс из точки, соответствующей 60 % Рb и 40 % Sb, восстанавливаем перпендикуляр до пересечения с отрезком ВС, получаем точку, которая соответствует критической температуре 350 °С — плавления (затвердевания) сплава 60 % Pb + 40 % Sb.
Таким образом, мы получили диаграмму состояния двухкомпонентного сплава свинец — сурьма. Все сплавы Рb— Sb независимо от массовой доли компонентов до температуры 245 °C имеют твердую фазу — механическая смесь. Сплав по линии DВЕ начинает медленно расплавляться при нагревании и затвердевает при охлаждении. Эту линию называют линией солидуса (от лат. solidus — твердый).
По линии АВС сплавы расплавляются при нагревании, при охлаждении начинают медленно кристаллизоваться. Эта линия называется линией ликвидуса (от лат. liquidus — жидкий). Между линиями DBE и линией АВС сплавы находятся в полужидком состоянии. Сплав с 87 % Рb и 13 % Sb имеет самую низкую температуру плавления (затвердевания). Этот сплав, так же как и чистые металлы, плавится при одной температуре. Такие сплавы получили название эвтектических сплавов.
Эвтектика — мелкодисперсная механическая смесь двух компонентов, образовавшаяся при температуре плавления (кристаллизации), значительно ниже температуры плавления сплавляемых компонентов в процессе затвердевания. Левее эвтектики сплавы называются доэвтектическими, правее — заэвтектическими.
Рассмотрим фазовые состояния сплава свинец — сурьма. Выше линии АВС сплав находится в жидком состоянии (жидкая фаза), между линией АВ и DB — в полужидком (Pb + жидкость). Ниже лини DB сплав состоит из механической смеси свинца и эвтектики. Между линиями ВС и ВЕ сплав будет иметь полужидкую фазу и кристаллы сурьмы. Ниже линии ВЕ сплав будет состоять из механической смеси (эвтектика и сурьма).
Диаграмма состояния сплава Pb — Sb относится к типу диаграмм, в которых сплавляемые компоненты неограниченно растворяются в жидком состоянии и не растворяются в твердом состоянии, образуя механические смеси (эвтектика).
Анализируя диаграмму состояния сплавов, можно изучить следующие характеристики: температуру плавления (кристаллизации), виды структур сплавов, способность образовывать ликвацию, режимы термообработки и обработки давлением. При изучении диаграмм состояния двухкомпонентных сплавов следует обращать внимание на превращение компонентов сплавов в кристаллическом (твердом) состоянии.
В связи с этим различают следующие особенности аллотропных изменений сплавов (типовые диаграммы состояния):
- диаграммы состояния первого рода — для сплавов, компоненты которых полностью растворяются в жидком состоянии, ограниченно растворяются в твердом состоянии и образуют механические смеси (Pb— Sb, Sn— Zn и др.);
- диаграммы состояния второго рода — для сплавов, компоненты которых полностью растворяются в жидком и твердом состоянии с образованием твердых растворов (Ag— Au, Cu— Ni; Fe— V и др.);
- диаграммы состояния третьего рода — для сплавов, компоненты которых неограниченно растворяются в жидком состоянии, практически не растворяются в твердом состоянии и образуют механические смеси (эвтектика) с полиморфным превращением (первичным и вторичным) структурно-фазового состава;
- диаграммы состояния четвертого рода — для сплавов, компоненты которых в жидком состоянии растворяются друг в друге, а в твердом состоянии образуют устойчивые или неустойчивые химические соединения.

