Содержание страницы
Современная металлургия и материаловедение немыслимы без понимания закономерностей фазовых превращений в сплавах. Ключевым инструментом, позволяющим анализировать, прогнозировать и управлять структурой и свойствами материалов, являются диаграммы состояния. Эти диаграммы — графическое представление фазового состава системы в зависимости от температуры и концентрации компонентов — позволяют не только оптимизировать состав сплавов, но и управлять процессами термообработки, литья и механической обработки. В данной работе рассмотрены основные типы диаграмм состояния двухкомпонентных систем, включая систему железо-углерод, как важнейшую для машиностроения и металлургии. Также затронуты принципы фазовых превращений, критические точки и структура различных типов сталей и чугунов.
Первое осознанное представление о фазовых превращениях в твердых телах возникло в конце XIX века, благодаря трудам русских и западноевропейских ученых. Значительный вклад в развитие теории фазовых превращений внёс русский химик Николай Семёнович Курнаков, разработавший основы фазового анализа и предложивший системный подход к построению диаграмм состояния. Именно его имя ассоциируется с правилом Курнакова, связывающим свойства сплавов с типом фазовых диаграмм. В XX веке диаграмма состояния системы Fe–C была подробно исследована и стандартизирована, став краеугольным камнем при разработке сталей и чугунов. Эти диаграммы легли в основу не только металлургических расчётов, но и учебных программ технических вузов.
1. Диаграммы состояния двухкомпонентных систем. Фазы, структуры
В основе большинства современных технических материалов лежат сплавы, включающие два и более химических элемента, которые называются компонентами. Характеристики таких материалов формируются за счёт присутствующих в них фаз и их пропорционального соотношения.
Графическое отображение изменений фазового состояния в зависимости от температуры и состава компонентов известно как диаграмма состояния (см. рис. 1, рис. 2). Эти диаграммы позволяют строить предельно точные прогнозы поведения сплавов при различных технологических воздействиях.
Фазой называется структурный участок сплава, обладающий однородностью по составу, атомной упаковке и имеющий чёткие границы отделения от других фаз.
Система – это множество фаз, находящихся во взаимодействии и образующих единое физико-химическое целое – сплав.
- по диаграмме можно определить, какая структура формируется при различных режимах охлаждения;
- определяется температура, наиболее подходящая для заливки сплава в форму при литье;
- оценка склонности к химической неоднородности и текучести жидкого металла становится возможной;
- анализируются условия пригодности материала для обработки под давлением;
- устанавливается подходящий режим термообработки конкретного состава.
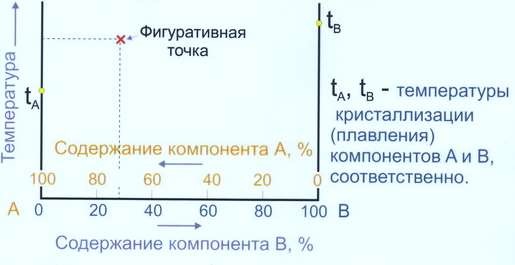
Рис. 1. Метод построения диаграмм состояния
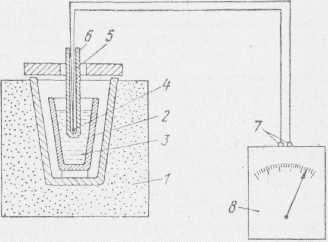
Рис. 2. Экспериментальная установка для построения диаграмм состояния, где: 1 – печь; 2 – тигель; 3 – расплавленный металл; 4 – горячий спай; 5 – термопара; 6 – колпачок; 7 – холодный спай; 8 – гальванометр
Чтобы подтвердить достоверность диаграммы, используют правило фаз, которое позволяет описать направление фазовых превращений в условиях достижения равновесия.
Это правило даёт возможность:
- предвидеть фазовые изменения при изменениях температуры;
- выяснить, осуществляется ли кристаллизация при определённой температуре или в температурном диапазоне;
- установить, сколько фаз способно одновременно сосуществовать при заданных условиях.
Математическая формулировка правила фаз выглядит следующим образом:
С = К + 1 – Ф
где: К – число компонентов, Ф – число фаз в системе, С – количество степеней свободы (вариантность).
Степени свободы определяются как количество факторов (внутренних или внешних), которые можно менять независимо, не вызывая изменений числа присутствующих фаз.
Пример диаграммы, где компоненты способны полностью растворяться как в жидком, так и в твёрдом виде, представлен на рис. 3.
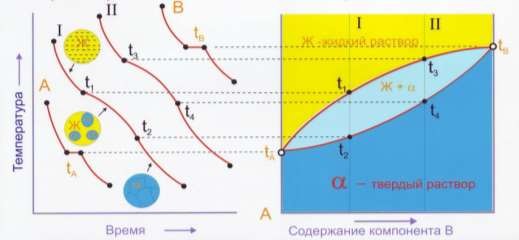
Рис. 3. Диаграмма состояния с полной растворимостью компонентов в твёрдой и жидкой фазах
Анализируя диаграмму состояния, можно определить, какие фазы будут присутствовать при заданной температуре, и вычислить их количественное соотношение.
Для этого применяются два основополагающих принципа (рис. 4):
- Метод определения состава фаз – правило концентраций;
- Метод расчёта количественного соотношения фаз – правило отрезков.
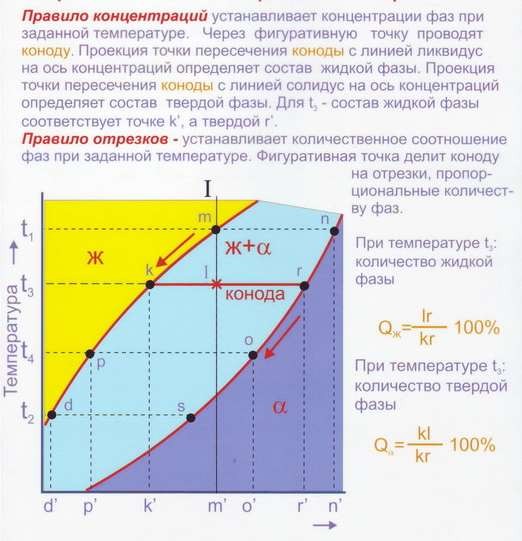
Рис. 4. Использование правила концентраций и отрезков при анализе диаграмм состояния
При частичной растворимости компонентов в твёрдой фазе и образовании эвтектической структуры, применяется другой тип диаграммы (рис. 5):
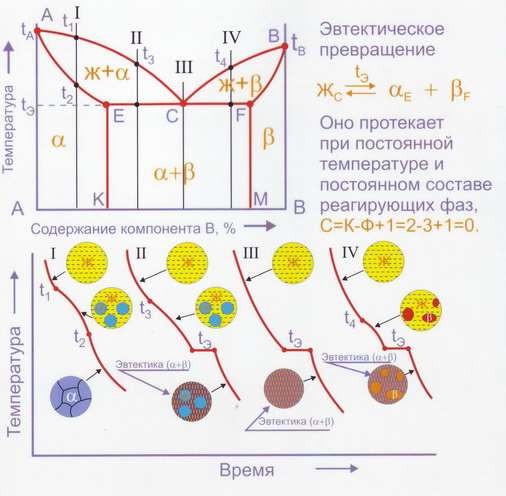
Рис. 5. Диаграмма состояния с ограниченной растворимостью и эвтектикой: построение кривых охлаждения
Если растворимость компонентов переменна и ограниченна в твёрдом состоянии, диаграммы имеют иную форму (рис. 6):
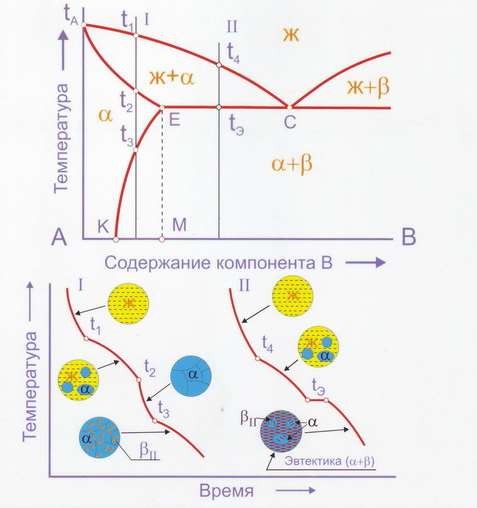
Рис. 6. Пример построения диаграммы при переменной растворимости компонентов
Существуют диаграммы, где ограниченная растворимость сопровождается образованием перитектической реакции (рис. 7):
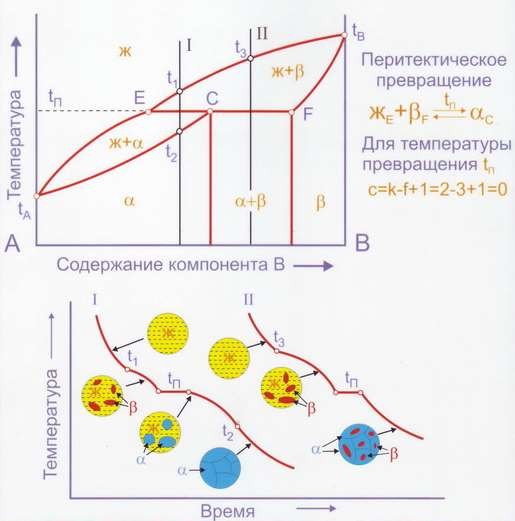
Рис. 7. Диаграмма состояния с перитектической реакцией
В системах с полиморфными превращениями и эвтектоидными реакциями формируются особые диаграммы (рис. 8):
Эвтектойдное превращение: γЕ → αК + βF
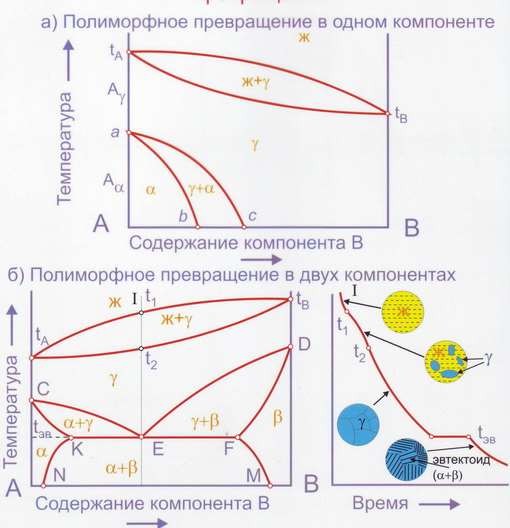
Рис. 8. Кривые охлаждения для сплавов с полиморфными превращениями
Некоторые компоненты в сплавах способны формировать устойчивые химические соединения, что также отражается в диаграммах состояния (рис. 9):
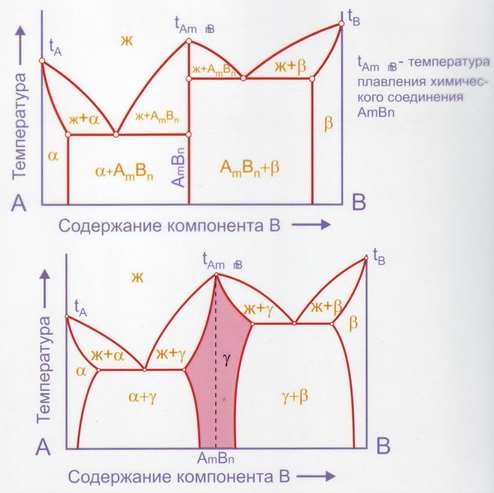
Рис. 9. Диаграмма с образованием химических соединений между компонентами
Физико-механические характеристики сплавов в условиях равновесия напрямую определяются тем, какие фазы в них образуются. Диаграммы состояния позволяют прогнозировать свойства конечного продукта на всех стадиях его формирования (рис. 10).
Наиболее технологичными считаются сплавы с твёрдыми растворами – они поддаются пластической деформации, но при этом имеют низкие литейные характеристики. В противоположность им, эвтектические сплавы обладают превосходной жидкотекучестью, но хуже обрабатываются резанием.
Промежуточные фазы, такие как карбиды, нитриды, бориды и оксиды, зачастую характеризуются значительной хрупкостью и высокой температурой плавления.
Фундаментальные зависимости между составом сплавов и их свойствами, обнаруженные Н.С. Курнаковым, активно используются при разработке новых материалов.
Кроме классификации по химической связи, кристаллы также подразделяются по типу кристаллической решётки, что даёт возможность заранее предсказывать изменения свойств при варьировании состава.
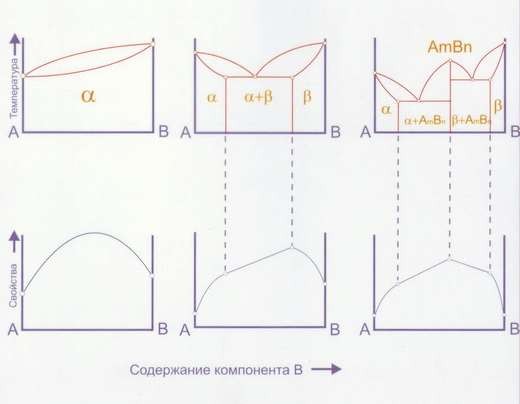
Рис. 10. Взаимосвязь между свойствами сплавов и типами диаграмм, основанная на принципах Н.С. Курнакова
2. Диаграмма состояния системы железо – углерод (Fe – Fe3C)
Среди большого числа диаграмм состояния различных сплавов наибольшее практическое значение имеет диаграмма состояния системы железо – углерод, представленная на рисунке 11. Это обусловлено широчайшим распространением и применением железоуглеродистых сплавов в промышленности, строительстве и машиностроении, начиная от низкоуглеродистых сталей до чугунов различных марок.
Существует два основных варианта диаграммы состояния для системы Fe – C:
- метастабильная система Fe – Fe3C (с участием цементита);
- стабильная система Fe – графит (Гр.), где углерод представлен в виде графита.
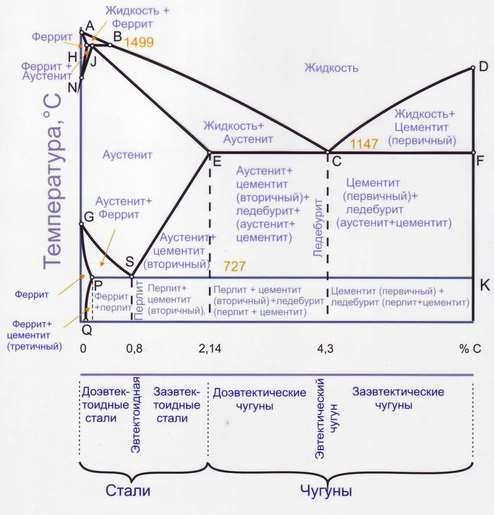
Рис. 11. Диаграмма фазовых превращений железо – углерод
Железо и углерод в данной системе рассматриваются как основные химические компоненты. Чистое железо плавится при температуре 1539оС и способно существовать в нескольких кристаллических формах (модификациях), в зависимости от температуры.
Форма Feα характеризуется объемно-центрированной кубической (ОЦК) решёткой и существует при температурах до 911оС, а также в интервале от 1392 до 1539оС. Существенной особенностью данной модификации является проявление ферромагнитных свойств при температурах ниже 768оС. Эта точка известна как температура Кюри.
Модификация Feγ имеет гранецентрированную кубическую (ГЦК) решётку, устойчива в температурном диапазоне от 911 до 1392оС и характеризуется парамагнетизмом. При переходе из Feα в Feγ происходит уменьшение объема кристаллической решетки примерно на 1%. Сам процесс перехода между ОЦК и ГЦК решётками носит название полиморфное превращение.
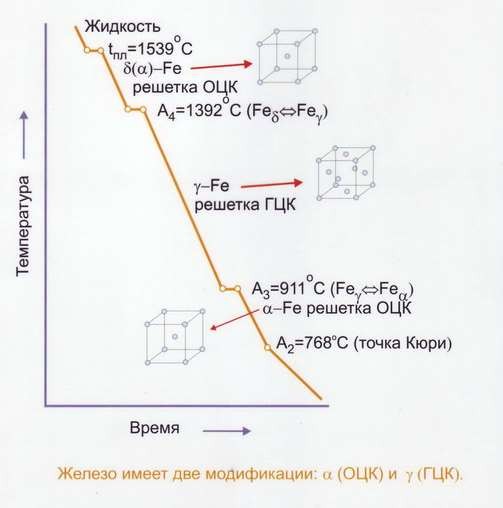
Рис. 12. Температурные области устойчивости различных модификаций железа
Углерод в системе может существовать в двух аллотропических формах: в виде кристаллического графита, устойчивого при обычных условиях, и в форме алмаза, стабильной при высоких давлениях и температурах.
В диаграмме Fe – C идентифицируются следующие фазы (рис. 13 и рис. 14):
- жидкий однородный расплав;
- феррит (Ф) — твердое решение углерода в α-железе;
- аустенит (А) — твердое решение углерода в γ-железе;
- цементит (Ц) — химическое соединение Fe3C;
- свободный углерод в виде графита (Гр.).
Фазовый состав железоуглеродистых сплавов

Рис. 13. Фазовая составляющая железо – углеродной системы


Рис. 14. Структура кристаллических решёток: a – алмаз, б – графит, в – цементит
Процессы кристаллизации в системе сопровождаются фазовыми превращениями, происходящими при строго определённых температурах.
Первая критическая линия — линия ликвидуса (ABCД на рис. 11) — отражает начало кристаллизации из расплава.
Вторая критическая линия — линия солидуса (AHJECF) — показывает завершение кристаллизации.
По содержанию углерода сплавы делятся на две основные группы:
- стали — содержание углерода до 2,14% включительно;
- чугуны — концентрация углерода превышает 2,14%.
В данной системе возможны следующие изотермические превращения:
- в сталях — перитектическое и эвтектоидное (рис. 15–17);
- в чугунах — эвтектическое (рис. 22).
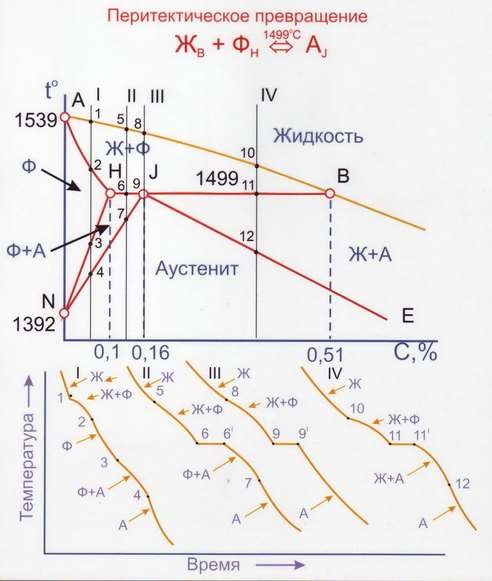
Рис. 15. Охлаждение сталей с перитектическим превращением
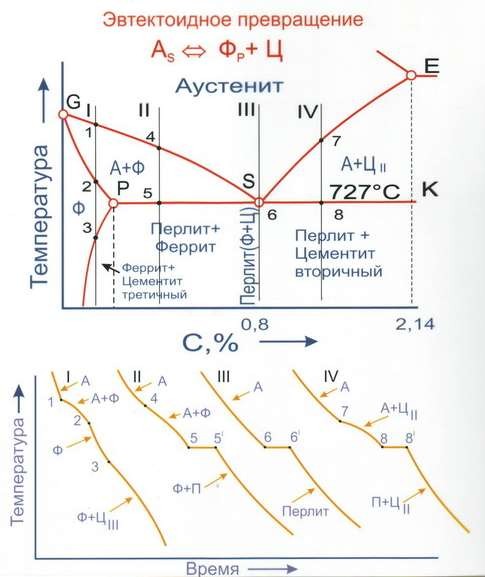
Рис. 16. Охлаждение сталей с эвтектойдным превращением
Наибольший интерес в металлургической практике представляют превращения, протекающие в твёрдом состоянии при температурах ниже линии NJE (рис. 17), так как большинство технологических процессов — таких как термическая обработка и ковка — происходят именно в этом интервале температур.
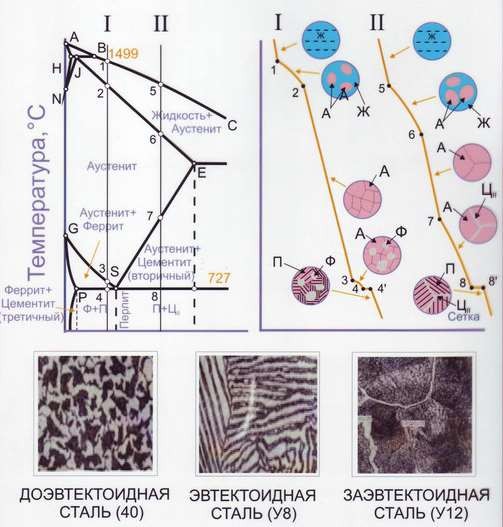
Рис. 17. Структурные изменения сталей в процессе охлаждения
Для примера рассмотрим конкретные марки сталей:
- Сталь 40: углеродистая конструкционная, содержит около 0,40% C, структура — феррит + перлит;
- У8: инструментальная сталь с 0,8% C, структура — пластинчатый перлит;
- У12: инструментальная высокоуглеродистая сталь с 1,2% C, структура — перлит + третичный цементит.
Цементит различают по происхождению:
первичный — выделяется из жидкой фазы,
вторичный — образуется из аустенита,
третичный — формируется из феррита.
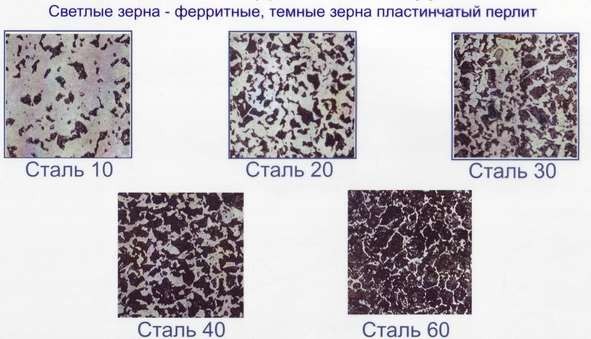
Рис. 18. Микроструктуры доэвтектойдных сталей

Рис. 19. Эволюция микроструктур эвтектоидных и заэвтектоидных сталей
Существуют и другие важные обозначения критических точек на диаграмме Fe – C, представленные на рисунке 20.

Рис. 20. Ключевые критические точки фазовых превращений
На свойства сталей сильное воздействие оказывают не только содержание углерода, но и легирующие примеси, а также температурные условия (рис. 21).
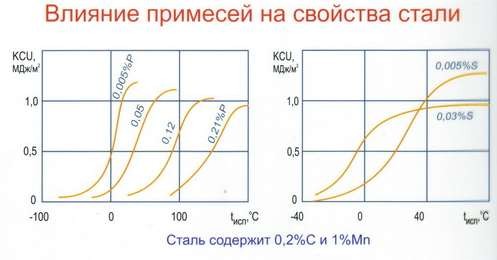
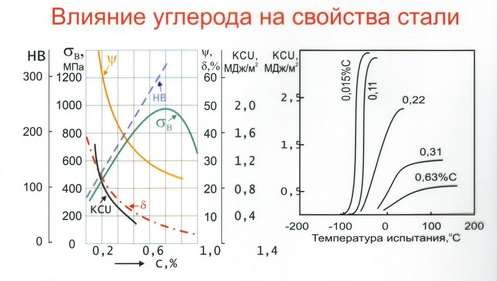
Рис. 21. Механические характеристики сталей в зависимости от состава
Железоуглеродистые сплавы с эвтектическим превращением (чугуны)
Чугун — это сплав, содержащий более 2,14% углерода. При его кристаллизации происходит изотермическое эвтектическое превращение (рис. 22).
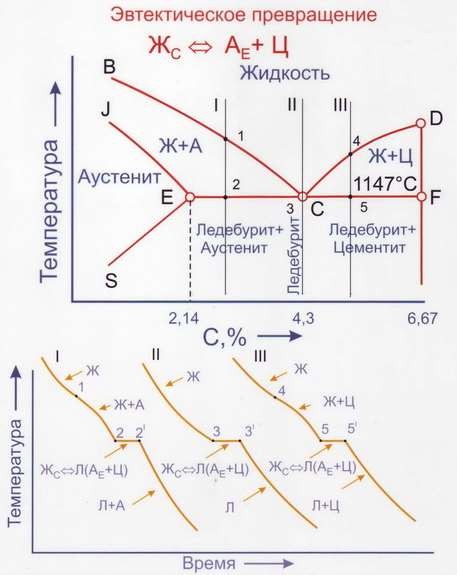
Рис. 22. Процессы кристаллизации чугунов
Эвтектический чугун с содержанием 4,3% C при температуре 1147оС кристаллизуется в виде смеси аустенита и цементита. Эта смесь носит название ледебурит (рис. 23).
При дальнейшем охлаждении концентрация углерода в аустените изменяется по линии ЕS вследствие выделения вторичного цементита и к температуре эвтектойдного превращения принимает значение 0,8%. При температуре линии РSК аустенит в ледебурите претерпевает эвтектойдное превращение в перлит.
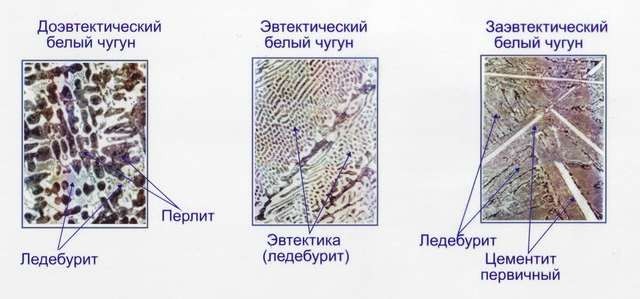
Рис. 23. Микроструктуры белых чугунов Железоуглеродистые сплавы могут кристаллизоваться в соответствии с
диаграммой железо – графит только при весьма медленном охлаждении и наличии графитизирующих добавок Si, Ni, и др. (рис. 24). Такие сплавы называют серыми чугунами (рис. 25).
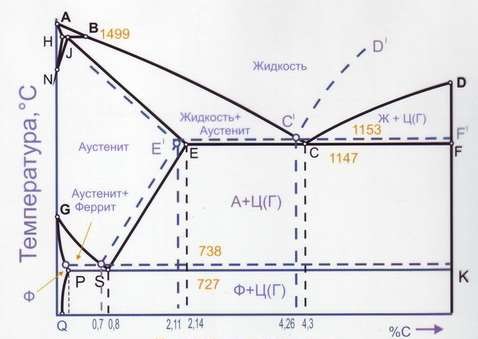
Рис. 24. Диаграмма состояния системы железо – графит
В зависимости от формы графитных включений серые чугуны называют: обычный серый чугун, ковкий чугун и высокопрочный чугун (рис. 25).

Рис. 25. Структура серых чугунов
На рис. 26, 27 и 28 показана маркировка и металлическая основа серых чугунов.
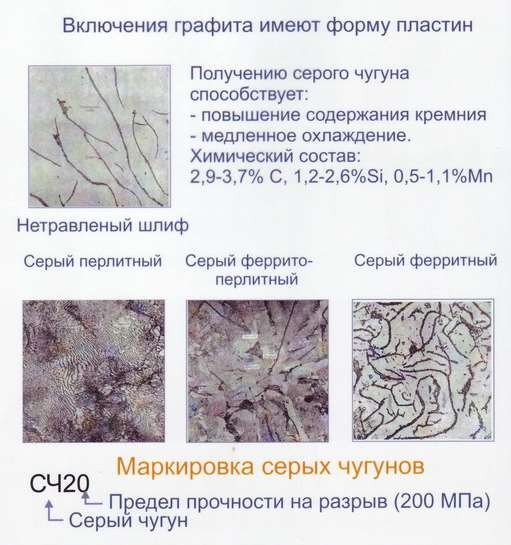
Рис. 26. Микроструктура и маркировка серых чугунов
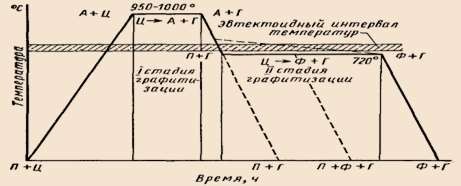

Рис. 27. Режим графитизации белых чугунов, микроструктура и маркировка ковких чугунов
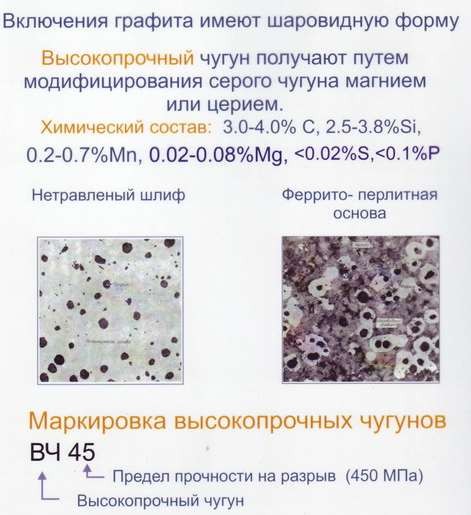
Рис. 28. Микроструктура и маркировка высокопрочных чугунов
Ковкие чугуны получают путём отжига белого чугуна, такой отжиг называют – графитизацией белых чугунов. Графитизация делится на несколько стадий в процессе которых цементит полностью распадается на графит.
На рис. 29 изображены структуры железоуглеродистых сплавов (феррит – а, доэвтектойдные стали –б, в, эвтектойдная – г, структуры белых чугунов – е, ж, з)
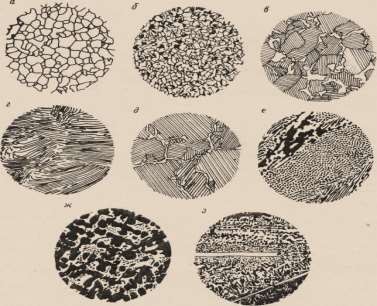
Рис. 29. Микроструктуры в железо – углеродистых сплавах
Заключение
Интересные факты:
-
Диаграмма Fe–C — одна из наиболее изученных и применяемых в технике. Она позволяет точно предсказать структуру стали после охлаждения, что критически важно в машиностроении.
-
Эвтектическая температура для чугуна составляет 1147 °C — при этой температуре из расплава одновременно образуются аустенит и цементит.
-
Точка Кюри (768 °C) — температура, выше которой феррит теряет магнитные свойства, что важно при термообработке и применении магнитных сталей.
-
Цементит, фаза Fe₃C, обладает твёрдостью порядка 800–900 HV, но при этом чрезвычайно хрупок.
-
Название «ледебурит» получила структура, названная в честь австрийского металлурга Адольфа Ледебура, впервые описавшего эвтектические превращения в чугуне.
Диаграммы состояния — это мощный инструмент, объединяющий в себе принципы термодинамики, фазовой теории и прикладной металлургии. Их использование позволяет не только описывать существующие сплавы, но и создавать новые материалы с заранее заданными свойствами. Система Fe–C, будучи основой для производства сталей и чугунов, демонстрирует всю полноту многообразия фазовых превращений — от простых растворов до сложных эвтектических и перитектических структур.
