Содержание страницы
Наносенсорами называются аналитические устройства, содержащие чувствительные наноэлементы, воспринимающие и преобразующие параметры анализируемого объекта в пригодный для практического использования сигнал, обычно электрический, хотя возможно и иной по природе, например, оптический сигнал.
По типу анализируемых объектов (воспринимаемых и преобразуемых параметров) наносенсоры подразделяются на три основных класса: физические наносенсоры – детектируют физические параметры анализируемых объектов; химические наносенсоры – детектируют химический состав анализируемых объектов, наличие химических веществ в окружающей среде; биологические наносенсоры (бионаносенсоры) – детектируют физиологическое состояние анализируемых объектов, наличие биологических веществ в окружающей среде.
При создании наносенсоров широко используются разнообразные наноматериалы, обладающие интеллектуальными свойствами.
Физические и химические наносенсоры
Для контроля температуры применяются наносенсоры в виде пленок на основе многостенных углеродных нанотрубок, характеризующихся температурной зависимостью проводимости.
Для контроля влажности применяются керамические наносенсоры, действие которых основано на зависимости электропроводности керамики от влажности. Наиболее эффективно использовать наносенсоры на основе нанопористой керамики, так как они характеризуются высокой чувствительностью благодаря большой площади поверхности, доступной для адсорбции воды. В этом отношении особенно перспективны нанопористые пленки оксида алюминия (рис. 1). Наносенсоры подобного типа также могут использоваться для контроля содержания аммиака в потребляемой растениями воде.

Рис. 1. Типичный вид сенсора влажности (а) на основе пленки из нанопористого оксида алюминия (б): а – масштаб метки 1 мм; б – средний диаметр пор 22,7 нм
Для определения химического состава газовых сред применяются наносенсоры, конструкцию которых составляют изолирующая подложка, размещаемая на подложке пластинка нагревательного элемента и нанесенная на пластинку нанопленка из полианилина (рис. 2). Принцип действия таких наносенсоров состоит в том, что проводимость полианилиновой пленки при нагревании меняется в зависимости от состава газовой смеси, молекулы которой адсорбируются полианилином.
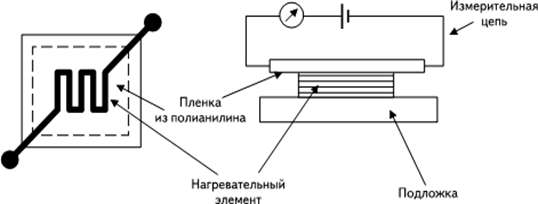
Рис. 2. Схема сенсора на основе нанопленки полианилина
Для определения химического состава газовых и жидких сред применяются наносенсоры на основе кремниевой нанопроволоки (рис. 3). Кремний, окисляясь на воздухе, покрывается слоем SiO2, в результате чего проводимость нанопроволоки меняется. Если поместить такую нанопроволоку в газовую или жидкую среду, то на этот слой будут осаждаться молекулы газа или растворенных в жидкости веществ, что также вызывает изменение проводимости нанопроволоки. В общем случае это изменение зависит от типа и количества осажденных молекул. Если же предварительно покрыть окисленную кремниевую нанопроволоку специально подобранным веществом, то полученный таким образом наносенсор будет детектировать строго определенные молекулы и характеристики анализируемой среды. Так, для создания рН-сенсора нанопроволока покрывается 3-аминопропил-этоксисиланом.
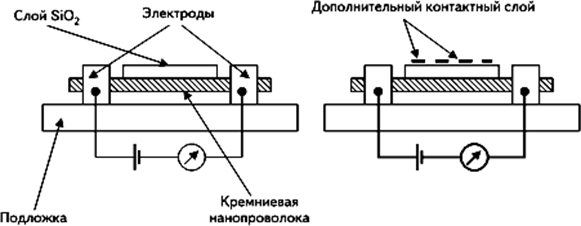
Рис. 3. Конструкция сенсора на основе кремниевой нанопроволоки
Весьма чувствительным газовым наносенсором является полевой транзистор на полупроводниковой нанотрубке. Так, эксперименты показывают, что если такой транзистор поместить в среду газа NО2, то проводимость нанотрубки повышается почти в три раза, о чем свидетельствует результаты сравнения вольтамперных характеристик транзистора до и после контакта с NО2. Такой эффект обусловлен тем, что при связывании NО2 нанотрубкой заряд переносится с нанотрубки на группу NО2, а это, в свою очередь, ведет к увеличению концентрации дырок в нанотрубке и ее проводимости.
Известны также газовые наносенсоры на основе углеродных нанотрубок, принцип действия которых связан с изменением термоЭДС или сопротивления при адсорбции молекул различных газов на поверхности нанотрубок. Разновидностью наносенсоров подобного типа является устройство, в котором адсорбция атомов газа на нанотрубках приводит к изменению частоты колебаний резонатора (рис. 28). Основной элемент такого наносенсора – резонансный контур, выполненный в виде проводящего диска из меди, покрытого слоем нанотрубок – однослойных (толщина слоя ~10 мкм) либо многослойных (толщина слоя ~100 мкм). При помещении наносенсора в камеру, наполненную газом (например, парами аммиака) происходит изменение резонансной частоты контура в результате адсорбции молекул газа на нанотрубке. Достоинство данного устройства состоит в малом времени восстановления прежней резонансной частоты после откачки газа из камеры (~10 мин).
Особый практический интерес представляют сенсорные наносистемы типа «электронный нос», включающие в себя блок оригинальных наносенсоров, аспирационное устройство, устройство регистрации сигналов и программное обеспечение распознавания обонятельных образов. Принцип работы таких приборов заключается в измерении электропроводности набора химических сенсоров при их взаимодействии с парами летучих веществ. В результате адсорбции молекул исследуемого вещества электропроводность чувствительных материалов сенсоров увеличивается. Каждый сенсор не является строго селективным по отношению к какому-либо газу. Однако величина отклика каждого сенсора из набора на разные газы индивидуальна. Математическая обработка данных сенсорного массива позволяет сформировать уникальный химический образ анализируемого вещества. Приборы такого типа эффективно использовать в антитеррористических целях для анализа сверхнизких концентраций взрывчатых, наркотических и других запрещенных к распространению веществ.
Важной областью применения физических и химических наносенсоров является сельское хозяйство. Для регулирования передачи тепловой энергии и воды между земной поверхностью и атмосферой посредством испарения и транспортных процессов в растениях важно контролировать температуру и влажность почвы. Поскольку вода имеет первостепенное значение в сельском хозяйстве, то для управления ирригацией необходимо получать точные сведения о влажности почвы на уровне корневой системы растений. Традиционные средства контроля температуры и влажности почвы не в состоянии достаточно точно определять температурные и влажностные профили. К тому же они громоздки и дороги. Вместо них можно эффективно применять сравнительно дешевые наносенсоры температуры и влажности. В частности, контроль потребности растений во влаге в полевых условиях может осуществляться с помощью специальных наносенсоров, размещаемых на листьях растений. Такие наносенсоры могут преобразовывать получаемую информацию о содержании влаги в электрические сигналы, которые передаются по каналам радиосвязи на пульт оператора.
Бионаносенсоры
Биосенсорами называются аналитические устройства, использующие биологические материалы для распознавания определенных молекул и выдающие информацию об их присутствии и количестве в виде определенного регистрируемого сигнала.
Впервые идею создания таких устройств высказал американский ученый Л. Кларк в 1960-е годы. Эта идея состояла в использовании ферментного электрода, т.е. электрохимического датчика с иммобилизованным на его поверхности ферментом. За прошедшие десятилетия эта идея получила значительное развитие. На сегодняшний день созданы и получили практическое применение разные типы биосенсоров. Большинство их используется для анализа биологических жидкостей.
Биосенсор состоит из двух основных функциональных элементов: биохимического и физического преобразователей (трансдьюсеров), находящихся в тесном контакте друг с другом (рис. 4). Биохимический преобразователь представляет собой слой из биоселектирующего материала, непосредственно реагирующего на присутствие определяемого компонента (субстрата) в многокомпонентной смеси. В качестве такого биоматериала используются разнообразные биологические структуры: ферменты, антитела, рецепторы, нуклеиновые кислоты и даже живые клетки. Биохимический преобразователь выполняет функцию биологического элемента распознавания. Он генерирует сигнал, функционально связанный с концентрацией определяемого компонента. В свою очередь, физический преобразователь трансформирует полученный концентрационный сигнал в электрический или иной более удобный для измерения сигнал (например, оптический), который регистрируется и обрабатывается с помощью специальной аппаратуры. Существуют различные виды физических преобразователей: электрохимические, оптические, термические, пьезоэлектрические и т.п.
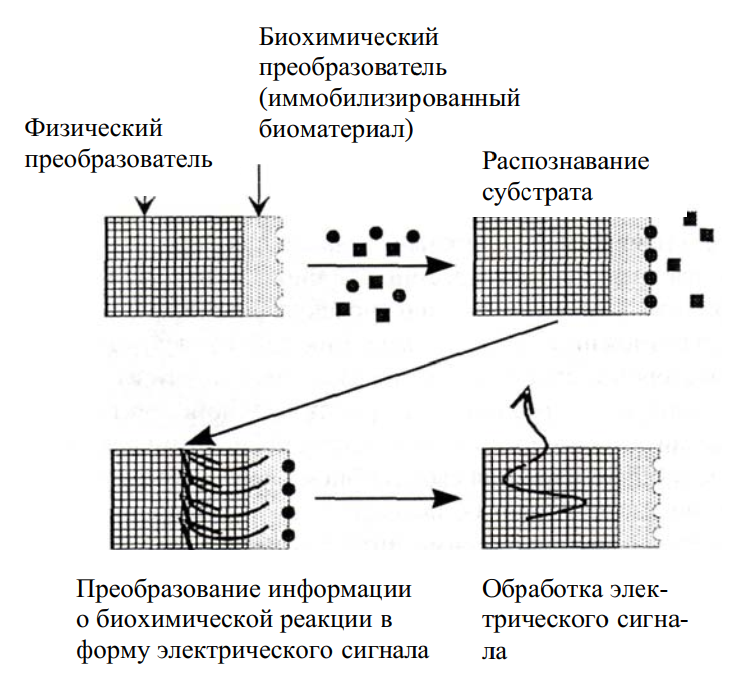
Рис. 4. Схема действия биосенсора
Наибольшее распространение получили электрохимические преобразователи. Одни из них генерируют потенциал на специальном электроде, на поверхность которого нанесен слой биоматериала, другие генерируют электрический ток реакции продукта превращения определяемого вещества на поверхности электрода, вызванного биоматериалом (в первом случае биосенсоры являются потенциометрическими, во втором – амперометрическими).
Таким образом, благодаря биосенсорам реализуется принципиально новый способ получения информации о химическом составе раствора. Наличие в устройстве биоматериала с уникальными свойствами позволяет с высокой селективностью определять нужные соединения в сложной по составу смеси, не прибегая ни к каким дополнительным операциям, связанным с использованием других реагентов.
Комбинируя различные биохимические и физические преобразователи, можно создавать большое число различных типов биосенсоров. Особенно большим числом конструктивных разновидностей характеризуются бионаносенсоры. С помощью бионаносенсоров можно с высокой точностью регистрировать параметры объектов, локализованных в очень малых объемах. Например, бионаносенсоры могут свободно циркулировать в потоке крови, скапливаясь вблизи клеток-мишеней или возле определенных молекул, обнаруживая генетические дефекты в ДНК, молекулы токсических веществ или поврежденные клетки. Бионаносенсоры позволяют не только отслеживать состояние живого организма, но также, в случае острой необходимости (например, при резком ухудшении состояния здоровья), автоматически выполнить некоторые требуемые действия, например, «обращаться» к врачу и вводить в организм по полученным рекомендациям требуемые лекарства.
Важной особенностью биосенсоров является лежащий в основе их действия механизм биомолекулярного распознавания (такие биосенсоры иначе называют иммуносенсорами). Сложность создания бионаносенсоров, действующих по принципу биораспознавания, связана с трудностью обеспечения их длительного и надежного функционирования, так как биоэлементы обычно быстро теряют способность к биораспознаванию. В связи с этим необходимо, прежде всего, научиться синтезировать молекулы, надолго сохраняющие заданные избирательность и химическое сродство.
Наиболее широкое распространение получили бионаносенсоры на основе ферментов (ферментные биосенсоры).
Ферменты, иначе называемые энзимами, – это узкоспециализированные по своему действию вещества, которые по своей природе являются белками. Ферменты осуществляют превращения веществ в организме, направляя и регулируя тем самым его обмен веществ. Они обладают оптимальной активностью при некоторых определенных условиях.
Ферментативный катализ обеспечивает биоселектирующими возможностями большинство бионаносенсоров. Сопряжение ферментативно-каталитических и электрохимических реакций, происходящих на электропроводящих материалах, погруженных в раствор электролита, позволило создавать биосенсоры для определения глюкозы, аминокислот, молочного сахара, мочевины и других метаболитов.
Наиболее удобно проводить измерения на ферментных электродах в амперометрическом режиме, т.е. измерять силу тока через поверхность электрода. При этом сила тока может быть однозначно связана с концентрацией измеряемого компонента.
Одним из самых распространенных является амперометрический бионаносенсор на основе иммобилизованной глюкозоксидазы для определения сахара в крови. Ток восстановления кислорода на катоде бионаносенсора прямо пропорционален концентрации кислорода. В присутствии субстрата (например, глюкозы в крови, взятой для анализа) ферментативная реакция понижает концентрацию кислорода. Соответственно, ток восстановления кислорода уменьшается пропорционально концентрации субстрата:
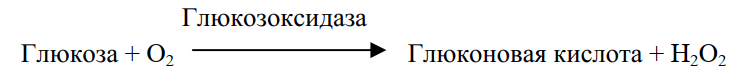
Преимущество данного типа бионаносенсора заключается в его высокой селективности, обусловленной высокой специфичностью глюкозоксидазы и природой электрохимической реакции, в которой участвуют компоненты ферментативного процесса.
Бионаносенсоры подобного типа, основанные на кислородном электроде как физическом преобразователе, позволяют определять кроме глюкозы и другие вещества: лактаты, салицилаты, оксалаты, L-аминокислоты и т.д.
При конструировании бионаносенсоров важно обеспечить увеличение продолжительности действия ферментов, поскольку они обычно сохраняют свои свойства лишь в течение относительно короткого времени. Для решения этой задачи используются специально разработанные операции иммобилизации ферментов, в ходе которых ферменты с помощью особых реагентов «закрепляются» либо на поверхности адсорбентов, например, силикагеля, угля или целлюлозы, либо вводятся в пленку пористого полимера, либо с помощью химических связей «пришиваются» к какой-либо подложке. При этом иммобилизованный фермент перестает быть подвижным, не вымывается из биослоя, а его каталитическое действие сохраняется. На рис. 5 схематически изображены основные способы иммобилизации ферментов в бионаносенсорах.
В последние годы все большее распространение находят клеточные бионаносенсоры. Их созданию способствовали достижения биотехнологии и биоинженерии, связанные с развитием методов включения живых клеток в полимеры и твердые носители различной природы.
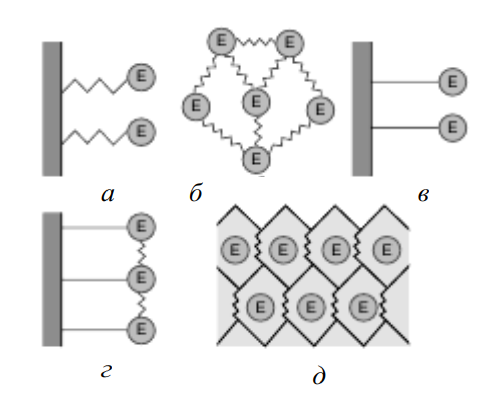
Рис. 5. Способы иммобилизации ферментов в биосенсорах: а – ковалентное связывание с поверхностью электрода; б – сшивание; в – адсорбция на носителе (электроде); г – ковалентное связывание и пришивание к подложке (электроду); д – захват носителем (в пленке полимера)
Биодетектирование, основанное на использовании клеток, является наиболее перспективным направлением развития бионаносенсорной техники, поскольку клетки имеют способность идентифицировать мельчайшую концентрацию агентов окружающей среды. Использование живых клеток в качестве сенсорных элементов обеспечивает возможность достижения высокой чувствительности к широкому кругу химически активных веществ, которые влияют на электрохимическую активность клеток. В частности, особого внимания заслуживают планарные микроэлектродные матрицы, позволяющие осуществлять запись внеклеточных сигналов от электрохимическиактивных клеток, культивируемых in vivo. Спектр внеклеточных сигналов может модулироваться, когда клетки помещаются в разнообразные химические или биологические агенты, и этот модулированный сигнал является характерным «образцом подписи» (служит в качестве «отпечатка пальца») специфического агента.
Клетки представляют собой доступный биологический материал. Широко используются клетки растений, животных, человека, но наибольшее применение находят клетки микроорганизмов, которые культивируются, легко воспроизводятся и поддерживаются в чистой культуре. В отличие от ферментов при использовании клеток не требуется дорогостоящих стадий очистки. При иммобилизации клетки сохраняют все наиболее важные структуры и проявляют большую стабильность. Для многих типов клеток, особенно микробных, разработаны эффективные методы генетических операций, дающие возможность получать мутанты с высоким содержанием того или иного белка или фермента, что позволяет оперировать с высокоэффективными каталитическими системами. Поскольку клетки сохраняют аппарат биосинтеза белка, то можно разрабатывать высокоэффективные методы генодиагностики.
Особенности метаболизма клеток дают возможность создавать биосенсоры как на индивидуальные молекулы, так и на очень широкие классы соединений, например, на всю совокупность биологически поглощаемых веществ. Для создания клеточных биосенсоров, так же как и ферментных, используются различные виды физических преобразователей.
Применения клеточных бионаносенсоров многообразны. Разработаны биосенсоры для селективного определения фенолов, пролина, глутамина, тирозина, молочной и аскорбиновой кислот, глюкозы, сульфат-иона, аммония и других веществ.
Существует метод определения биологического потребления кислорода – анализ на определение совокупности органических соединений, которые могут быть использованы микроорганизмами. Традиционно этот метод требует для получения необходимых данных несколько дней. Бионаносенсоры с иммобилизованными клетками позволяет получать эти же результаты в течение нескольких минут.
Особый интерес представляют так называемые микробные бионаносенсоры, действующие на основе использования иммобилизованных микроорганизмов. Примером таких устройств является нанобиосенсор на аммиак (в сточных водах), который можно эффективно применять при решении вопросов охраны окружающей среды, в частности, при контроле степени очистки промышленных стоков.
Нанотехнологии открывают широкие возможности в области создания бионаносенсоров с электрическим преобразовательным механизмом, обеспечивающих высокочувствительное восприятие биологических объектов, особенно нуклеиновых кислот и белков. К числу таких сенсоров относятся разнообразные аналитические устройства, создаваемые на основе углеродных нанотрубок и нанопроволок.
Биосенсоры на основе одностенных углеродных нанотрубок можно рассматривать как особый вид полевых транзисторов, выполненных на основе квази-одномерного наноматериала и характеризующихся сверхмалыми размерами, высоким отношением поверхность – объем и уникальными физико-химическими свойствами, что существенно отличает их от объемных аналогов. Действие обычных полевых транзисторов основано на управлении с помощью электрического поля проводимостью полупроводникового канала, который скрыт внутри конструкции транзистора. В отличие от обычных полевых транзисторов транспорт заряда в квазиодномерном наноматериале осуществляется при непосредственном контакте с окружающей средой и, как следствие, является крайне чувствительным к ее химическим или физическим воздействиям. Это явление наиболее заметно проявляется в одностенных углеродных нанотрубках, поскольку благодаря их уникальной однослойной атомарной структуре транспорт заряда через нанотрубки происходит по поверхности, непосредственно подвергающейся воздействию внешней среды. В общем случае одиночная биомолекула, находящаяся на поверхности или вблизи нанотрубки, способна изменять электронные свойства нанотрубки за счет: 1) передачи заряда между биомолекулой и нанотрубкой, 2) рассеяния потенциала, прикладываемого к движущимся зарядам и 3) рассеяния заряда, вызванного локальной деформацией.
Функционирование биосенсоров на основе одностенных углеродных нанотрубок обеспечивается благодаря иммобилизации биоагента нанотрубкой, которая происходит путем нековалентной адсорбции биоагента нанотрубкой или обвертывания биоагента вокруг нанотрубки либо путем ковалентного присоединения биоагента к функциональным группам, образующимся на каркасе нанотрубки в ходе химической реакции. С помощью указанных механизмов такие биосенсоры способны эффективно детектировать нуклеиновые кислоты и белки, а также клеточные патогенные бактерии (Escherichia coli, Salmonella typhimurium и др.). На рис. 6. демонстрируется принцип действия биосенсора на основе одностенной углеродной нанотрубки в случае, когда нанотрубка оказывается обернутой одноцепочечной молекулой ДНК, взаимодействие которой с нанотрубкой приводит к изменению электропроводности последней в результате ее допинга электронами.

Рис. 6. Одностенная углеродная нанотрубка, обернутая молекулой одноцепочечной ДНК

Рис. 7. Матрица из кремниевых нанопроволок
Полупроводниковые нанопроволочные биосенсоры изготавливают из нанопроволок на основе полупроводниковых элементов (Si, Ge и др.) или соединений (группы II–VI, III–V и IV–IV). Принцип их действия, так же как и биосенсоров на основе углеродных нанотрубок, основан на использовании полевого эффекта. Подобно биосенсорам на основе углеродных нанотрубок их можно применять для детектирования нуклеиновых кислот, белков и бактерий. Кроме того, они чувствительны к изменениям pH-растворов. На рис. 7 показан конструктивный вариант полупроводниковых нанопроволочных биосенсоров в виде системы Si-нанопроволок, с помощью которых можно эффективно определять вирусы гриппа и аденовирусы.
Для детектирования сложных биологических соединений, например, белков, можно применять рассмотренные выше бионаносенсоры на основе кремниевых нанопроволок с оболочкой SiO2. Для того чтобы обеспечить детектирование белка стрептовидина, оболочку из SiO2 следует покрыть бычьим альбумином, меченным биотинамидокапроилом, который является селективным рецептором для стрептовидина (рис. 8).
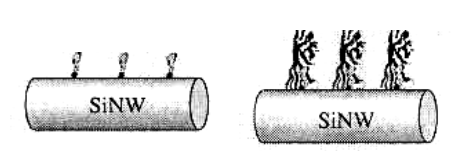
Рис. 8. Модифицированная кремниевая нанопроволока (слева) и присоединенный к ней стрептовидин
Осажденный на такую пленку стрептовидин меняет заряд на ее поверхности, а значит и проводимость нанопроволоки. Кремниевые нанопроволоки могут реагировать на концентрацию ионов кальция Ca2+, входящих в состав оболочки клеток и влияющих на метаболические процессы в живых организмах. Их применяют для детектирования ДНК, вирусов.
Особой конструкцией отличаются биосенсоры на основе нанокантилеверов. На рис. 9 показана схема биосенсора, основу конструкции которого составляет пара кантилеверов нанометровой толщины.
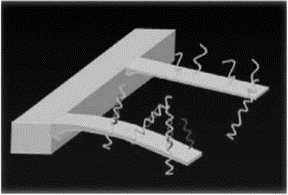
Рис. 9. Схема биосенсора на основе нанокантилеверов для детектирования молекулы ДНК
Между кантилеверами располагается молекула ДНК, которая вызывает их изгиб, регистрирующийся с помощью высокоразрешающего оптического дефлектора. В качестве кантилеверов преспективно использовать углеродные нанотрубки благодаря их уникальным механическим свойствам, а именно способности реверсивно изгибаться под действием ничтожно малой нагрузки.
Существуют разные типы конструкций биосенсоров на основе нанокантилеверов. Основная идея применения нанокантилеверов в качестве биосенсоров состоит в том, что биоматериал, адсорбированный на нанокантилевере, может изменять характеристики последнего. Это может быть изменение как массы (благодаря очень малой массе самого нанокантилевера), так и поверхностного напряжения. Соответственно, существуют два подхода к созданию биосенсоров на основе нанокантилеверов, соответственно, двух типов: резонансных и поверхностно-напряженных.
Действие резонансных нанокантилеверов основано на зависимости резонансной частоты их вибрации от величины присоединенной массы. Приложение переменного электрического напряжения между кантилевером и близлежащим электродом переводит кантилевер в возбужденное состояние и вызывает его вибрации, амплитуда которых может измеряться. Резонансная частота колебаний кантилевера изменяется с изменением присоединенной к нему массы, в частности, массы детектируемого вещества: чем меньше масса самого кантилевера, тем больше чувствительность к изменению массы. Резонансный нанокантилевер может использоваться в качестве биосенсора, способного детектировать одиночные молекулы.
Действие поверхностно-напряженных нанокантилеверов основано на зависимости угла отклонения (изгиба) кантилевера от величины его поверхностного напряжения. Осаждение молекул детектируемого вещества на поверхность одной из сторон кантилевера взывает изменение поверхностного напряжения, что приводит к изгибу кантилевера. Величина изгиба определяется с помощью близлежащего электрода или по отклонению лазерного луча, отраженного от поверхности кантилевера (подобно тому, как это имеет место в атомном силовом микроскопе). В последнем случае возможно разрешение до 1 ангстрема, что обеспечивает высокую чувствительность детектирования, которая будет тем выше, чем тоньше кантилевер.
Одним из перспективных подходов к созданию бионаносенсоров является применение техники оптоволоконного биозондирования. Действие оптоволоконных биозондов основано на принципах ближнепольной оптической микроскопии. Для детектирования используются оптические волокна с очень тонким наконечником (до 20 нм). Когда свет проходит через волокно, он создает затухающее электромагнитное поле в наконечнике, которое охватывает очень малый объем, поскольку его интенсивность падает экспоненциально с удалением от наконечника. Кроме того, это поле вызывает возбуждение преимущественно флуоресцентных частиц. Соответственно, техника оптоволоконного биозондирования используется в основном для детектирования биоагентов, снабженных флуоресцентными маркерами, в частности, для определения характера их распределения внутри клетки.
Возможен вариант применения данной техники, когда наконечник волокна покрывается антителами, которые способны связываться с антигенами – бактериями или вирусами (как известно, реакции антител с антигенами широко применяются в диагностике различных заболеваний). Техника оптоволоконного биозондирования предполагает пунктирование клеточной мембраны зондом, но, благодаря малому диаметру наконечника зонда, разрушение клетки не является губительным и клетки способны подвергаться дальнейшему клеточному делению (рис. 10).
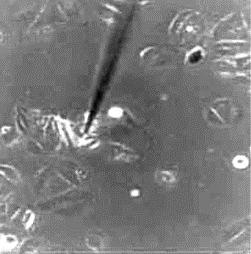
Рис. 10. Оптоволоконное биозондирование одиночной клетки
В последние годы в диагностической практике все более широкое применение получают кристаллические наночастицы ряда веществ, способные флюоресцировать. Такие нанокристаллы обладают высокой яркостью флюоресценции, обусловленной большим значением коэффициента поглощения, благодаря чему их можно детектировать как индивидуальные объекты с помощью обычных флуоресцентных микроскопов, что позволяет визуализировать процессы на уровне единичных молекул. Длина волны флуоресценции нанокристаллов зависит от их размеров, при этом для возбуждения нанокристаллов всех цветов достаточно одного источника излучения. Например, наночастицы селенида кадмия CdSe диаметром 3–6 нм могут возбуждаться источником света одной и той же длины волны, испуская при этом флуоресценцию в диапазоне от голубой до ближней инфракрасной области в зависимости от своего размера. Кроме того, нанокристаллы обладают высокой фотостабильностью, обеспечивая как возможность многократного увеличения мощности возбуждающего излучения, так и длительного (в течение дней или даже недель) отслеживания поведения метки в реальном времени. Такие уникальные свойства нанокристаллов позволяют использовать их в качестве идеальных флуорофоров в системах диагностики различных заболеваний, требующих регистрации многих параметров одновременно с целью установления точного диагноза.
Так как флуоресцентные нанокристаллы являются гидрофобными, то для биологических применений необходимо обеспечить их перевод в водную фазу, стабилизацию и конъюгацию с биомолекулами. Для этого нанокристаллы заключают в кремниевые оболочки, содержащие на своей поверхности тиольные, аминные или карбоксильные группы, либо в оболочки из полимеров, способных связываться с поверхностью наночастиц, обеспечивать их растворимость в водной фазе за счет полярных групп и содержащих дополнительные функциональные группы, доступные для конъюгации. Наночастицы, сконъюгированные с биомолекулами, могут использоваться во флуоресцентных методах селективной визуализации различных биологических объектов, включая вирусы.
Прогресс в области генной инженерии обеспечил значительные успехи в развитии биолюминесцентного анализа. На основе использования генов люминесцентной системы (так называемых luxгенов) ряда светящихся бактерий разработаны люминесцентные бионаносенсоры, обладающие высокой специфичностью. Такие биосенсоры имеют чувствительный слой, содержащий биологический материал (ферменты, ткани, бактерии, дрожжи, антигены/антитела, липосомы, органеллы, рецепторы, ДНК), который непосредственно реагирует на присутствие определяемого компонента и генерируют сигнал, функционально связанный с концентрацией этого компонента. Например, биосенсор на основе бактерий E.coli (кишечной палочки), определяет наличие в среде ртути, а на основе бактерий Pseudomonas putida (синегнойной палочки) – нафталина, толуола, ксилола.

